Aplastic anemia pathophysiology
Aplastic anemia Microchapters
Home
Patient Information
Overview
Historical Perspective
Classification
Pathophysiology
Causes
Differentiating Anemia aplástica de other Diseases
Epidemiology and Demographics
Risk Factors
Screening
Natural History, Complications and Prognosis
Diagnosis
Diagnostic Study of Choice
History and Symptoms
Physical Examination
Laboratory Findings
Electrocardiogram
Chest X Ray
CT
MRI
Echocardiography or Ultrasound
Other Imaging Findings
Other Diagnostic Studies
Treatment
Medical Therapy
Surgery
Primary Prevention
Secondary Prevention
Cost-Effectiveness of Therapy
Future or Investigational Therapies
Case Studies
Case #1
Aplastic anemia pathophysiology On the Web
Most recent articles
cited articles
Review articles
CME Programs
Powerpoint diapositivas
Imágenes
Sociedad Americana de Rayos Roentgen Imágenes de la fisiopatología de la anemia aplástica
Todas las imágenes X-rays Echo & Ultrasound CT Images MRI
Ongoing Trials at Clinical Trials.gov
US National Guidelines Clearinghouse
NICE Guidance
FDA sobre la fisiopatología de la anemia aplásica
El CDC sobre la fisiopatología de la anemia aplásica
La anemia aplásica anemia aplásica en las noticias
Blogs sobre anemia aplásica
Direcciones a los hospitales Tratamiento de la anemia aplásica
Calculadores de riesgo y factores de riesgo de la fisiopatología de la anemia aplásica
Editor-Jefe: C. Michael Gibson, M.S., M.D. ; Editor(es) Asociado(s) – Jefe: Priyamvada Singh, M.D. Nazia Fuad M.D.
Por favor, ayude a WikiDoc añadiendo contenido aquí. Es muy fácil. Haga clic aquí para aprender a editar.
Resumen
La médula ósea es un tejido esponjoso, que se encuentra dentro de las porciones esponjosas o esponjosas de los huesos. Está altamente vascularizada y ricamente inervada La médula ósea es el lugar primario de la hematopoyesis y está compuesta por células hematopoyéticas, tejido adiposo medular y células estromales. El rasgo más defenitivo en la fisiopatología de la anemia aplásica es la pérdida de células madre hematopoyéticas. Puede ser en forma de fallo hematopoyético o de destrucción de la médula ósea mediada por el sistema inmunitario. Los fármacos, las sustancias químicas, los virus y los diferentes tipos de mutaciones modifican el aspecto inmunológico de las CMH, lo que provoca la destrucción autoinmune de las células de la médula. La AA puede evolucionar gradualmente hacia otros trastornos hematológicos, como la hemoglobinuria paroxística nocturna, los síndromes mielodisplásicos y la leucemia mieloide aguda.) La evolución clonal en el AA puede producirse por mutaciones o anomalías citogenéticas. Los genes que se encuentran comúnmente mutados son DMNT3A, ASXL1, BCOR, BCORL1, PIGA.
Patofisiología
Fisiología
La fisiología normal de la médula ósea puede entenderse como sigue:
- La médula ósea es un tejido esponjoso, que se encuentra dentro de las porciones esponjosas o esponjosas de los huesos
- Está altamente vascularizada y ricamente inervada
- La médula ósea es el sitio primario de la hematopoyesis.
- Se compone de células hematopoyéticas, tejido adiposo medular y células estromales.
- Las células madre hematopoyéticas (HSC) de la médula ósea son la fuente de todas las células maduras de la sangre periférica y de los tejidos y son multipotentes.
- Las HSC se reconocen y aíslan según su inmunofenotipo.
- Las HSC constituyen una pequeña población dentro de la fracción CD34+/CD38 de las células de la médula ósea.
- La hematopoyesis está controlada por diversos mecanismos reguladores, incluidos los factores de crecimiento.
- La estructura normal de la médula ósea puede resultar dañada o desplazada por la anemia aplásica, las neoplasias o las infecciones.
- Esto conduce a la disminución de la producción de células sanguíneas y plaquetas.
Patogénesis
La característica más defensiva en la fisiopatología de la anemia aplásica es la pérdida de células madre hematopoyéticas.
Los mecanismos fisiopatológicos que dan lugar a la pérdida de CMH y causan anemia aplásica incluyen:
Fallo hematopoyético
- Las células CD34 están casi ausentes en la anemia aplásica.
- Las células progenitoras capaces de formar eritroides, mieloides y megacariocíticas están muy reducidas.
- Las células hematopoyéticas primitivas que están estrechamente relacionadas con las células madre son sistemáticamente deficientes.
- Los glóbulos blancos en la anemia aplásica tienen telómeros cortos.
- Los telómeros son repeticiones al final del cromosoma eucariótico y son esenciales para la protección del cromosoma y la replicación completa del ADN.
Destrucción de la médula por parte de las células T mediada por el sistema inmunitario
-
- Drogas, sustancias químicas, virus y diferentes tipos de mutaciones cambian el aspecto inmunológico de las CEH, lo que provoca la destrucción autoinmune de las células de la médula.
- En los pacientes con anemia aplásica adquirida, los linfocitos son los responsables de la destrucción de las células hematopoyéticas.
- Estos linfocitos T producen un factor inhibidor, interferones , factor de necrosis tumoral e interleucina-2, lo que provoca la muerte de las células hematopoyéticas por apoptosis.
- Las células T reguladoras CD4+CD25+FOXP3+ son deficientes en estos pacientes, de forma similar a lo que se observa en otras enfermedades autoinmunes.
- La deficiencia de estas células T reguladoras da lugar a un aumento de los niveles de la proteína T-bet en las células T, un aumento del interferón (IFN)-γ,2 y la destrucción de las células madre.
- El aumento de la respuesta inmunitaria, incluyendo el factor de necrosis tumoral -α, el IFNγ y la interleucina-6, son también muy comunes en los pacientes AA.
Evolución clonal
- La AA puede evolucionar gradualmente hacia otros trastornos hematológicos que incluyen
- Hemoglobinuria paroxística nocturna hemoglobinuria
- Síndromes mielodisplásicos
- Leucemia mieloide aguda
- La evolución clonal en los AA puede producirse por mutaciones o anomalías citogenéticas.
- Los genes que suelen estar mutados son
- DMNT3A
- ASXL1
- BCOR
- BCORL1
- PIGA
Genética
Los genes implicados en la patogénesis de la anemia aplásica son:
- HLA-DR15
- CD4+ CD25+ FOXP3+ células T reguladoras
- STAT3
- TERT
- TERC
Condiciones asociadas
La anemia aplásica se asocia con las siguientes condiciones:
- Anemia de Fanconi
- Hemoglobinuria Paroxística Nocturna
Patología Bruta
La anemia aplásica no no presenta ninguna patología macroscópica
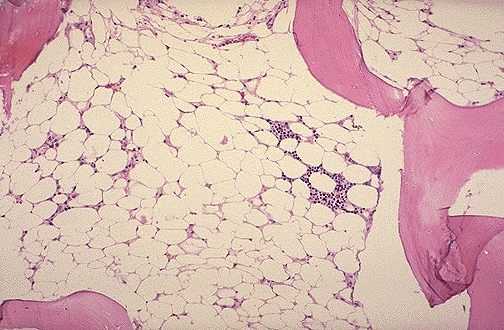
Patología microscópica
En la anemia aplásica la microscopía de la médula ósea revela hipo e incluso acelularidad, tejido adiposo y estroma pálido.
- Hays K (febrero de 1990). «Fisiología de la médula ósea normal». Semin Oncol Nurs. 6 (1): 3-8. PMID 2406826.
- Bacigalupo A (2007). «Anemia aplásica: patogénesis y tratamiento». Hematología Am Soc Hematol Educ Program: 23–8. doi:10.1182/asheducation-2007.1.23. PMID 18024605.
- 3.0 3.1 3.2 3.3 Brodsky, R. A. (2000). «Anemia aplástica: Pathophysiology and Treatment». Journal of the National Cancer Institute. 92 (9): 754-754. doi:10.1093/jnci/92.9.754. ISSN 1460-2105.
- 4.0 4.1 Young, Neal S. (2002). «Anemia aplástica adquirida». Annals of Internal Medicine. 136 (7): 534. doi:10.7326/0003-4819-136-7-200204020-00011. ISSN 0003-4819.