Az amnionmembrán felhasználása a szemészetben
2017. szeptember
Az amnionmembrán szövetek és sejtek kombinációjából áll, amely biológiai kötszerként használva segíti a sebgyógyulást azáltal, hogy a lágyszövetek újranövekedésének alapjául szolgál. Az amnion epiteliális és stromális rétegeiben található biológiailag aktív sejtek gyulladáscsökkentő, antibakteriális, antiimmunogén és antifibrotikus tulajdonságokkal rendelkező növekedési faktorokat és citokineket szállítanak1.
 A humán placentamembránokat először az 1900-as évek elején használták bőrpótlóként. Ezek az eljárások magukban foglalták az amnion- és a korionmembránt. Az amnionmembránt önmagában először 1940-ben alkalmazták a szemészetben, amikor De Rotth javasolta a szem égési sebének kezelésére.2 A kezelés sikeres volt, de az amnionmembrán használata ezután kiment a divatból egészen az 1990-es évek elejéig, amikor jobb feldolgozási és tárolási technikákat fejlesztettek ki.
A humán placentamembránokat először az 1900-as évek elején használták bőrpótlóként. Ezek az eljárások magukban foglalták az amnion- és a korionmembránt. Az amnionmembránt önmagában először 1940-ben alkalmazták a szemészetben, amikor De Rotth javasolta a szem égési sebének kezelésére.2 A kezelés sikeres volt, de az amnionmembrán használata ezután kiment a divatból egészen az 1990-es évek elejéig, amikor jobb feldolgozási és tárolási technikákat fejlesztettek ki.
Az elmúlt 25 év során szó szerint több ezer szemsebészeti eljárás során használtak amnionmembránt különböző szemészeti rendellenességek kezelésére, és több mint 700 lektorált cikket publikáltak. Az amnionmembránt különböző rekonstrukciós sebészeti eljárásokban is használták biológiai kötésként. Ezek az eljárások a következők: biológiai kötések égési sérülések és nem gyógyuló diabéteszes és vénás fekélyek esetén, hasi sérvek helyreállítása, a szívburok lezárása, valamint a sebészeti összenövések megelőzésére szolgáló gátként.3,4
A magzatmembrán anatómiája és fiziológiája
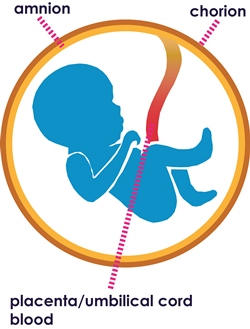
A magzatmembrán a méhen belül az extraembrionális szövetből fejlődik ki, amely magzati és anyai komponenseket egyaránt tartalmaz, amelyeket a chorionos villi tart össze. A magzati komponens a magzatburokból és a magzatmembránból áll, amely elválasztja a magzatot a méhnyálkahártyától4. Az amnionmembrán (AM) a méhlepény magzati membránjainak legbelső rétege. Avaszkuláris, és egy hámréteggel rendelkezik, amely alatt egy avaszkuláris stromális réteg található5,6.
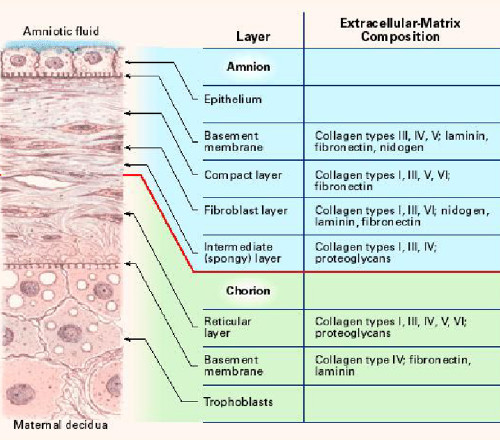 A magzatburok az egyik legvastagabb membrán az emberi szervezetben. A mellékelt ábra4 az emberi magzatmembrán keresztmetszetét mutatja be, feltüntetve öt rétegének biokémiai jellemzőit7:
A magzatburok az egyik legvastagabb membrán az emberi szervezetben. A mellékelt ábra4 az emberi magzatmembrán keresztmetszetét mutatja be, feltüntetve öt rétegének biokémiai jellemzőit7:
- kuboidális hámréteg;
- alaphártya;
- kompakt réteg;
- fibroblaszt réteg; és
- középső (szivacsos) réteg.
Hogyan befolyásolja a magzatmembrán a gyógyulást
A magzatmembrán bazálmembránja egy vékony, retikuláris rostokból álló réteg, amely szorosan tapad a magzathámhoz, míg a szomszédos kompakt réteg sűrűbb és sejtektől mentes, összetett retikuláris hálózatból álló sejtekből áll.3,4 Alacsony immunogén potenciállal rendelkezik, és olyan bioaktív faktorokat tartalmaz, amelyekről bebizonyosodott, hogy előnyösek a sebkezelésben, mint például: kollagén, sejtadhéziós bioaktív faktorok (fibronectin, lamininek, proteoglikánok és glikozaminoglikánok) és növekedési faktorok.3,7
A magzatmembránban található biológiai faktorokból és citokinekből származó terápiás előnyök:
- Gyulladáscsökkentő hatások – A magzatmembrán elnyomja a pro-inflammatorikus citokineket.
- Antimikrobiális – Az amnionmembrán fizikai gátként szolgál a külső környezettel szemben a membrán szoros tapadásával a sebfelülethez, valamint antimikrobiális citokineket termel.
- Anti-scarring és antiadhéziós hatás – Az amnionmembrán a TIMP-k (tissue inhibitors of metalloproteinases) kiválasztásán keresztül csökkenti a proteáz aktivitást, ezért anti-fibrotikus hatású. A fibroblasztok aktiválásáért felelős TGF-ß-t is lecsökkenti, és megakadályozza a sérült felületek egymáshoz tapadását.
- Nem immunogén és alacsony antigénhatás – Az amnionnak alacsony a hisztokompatibilitási (HLA II. osztály) A, B, C DR vagy béta2 mikroglobulin antigének expressziója, ezért allogén kötszerként minden probléma nélkül használható.
- Fájdalomcsillapító tulajdonságok – Az idegvégződések hatékony lefedésének köszönhetően gyors fájdalomcsillapítás tapasztalható.
- Anti-angiogén – Megakadályozza az új erek kialakulását.
- IV, V és VII típusú kollagént tartalmaz – Ezek elősegítik a sejtek differenciálódását és tapadását.
- Epithelizáció elősegítése – Az alapmembrán jó szubsztrátum a sejtvándorláshoz és a hámsejtek polaritásának fenntartásához. Az olyan növekedési faktorok, mint a KGF, b-FGF, HGF és TGF-ß expressziójával együtt elősegíti a hámosodást, a sejtproliferációt és a differenciálódást.
Összefoglalva, a magzatmembrán hatásmechanizmusa a citokinek és növekedési faktorok magas koncentrációján alapul. A magzatmembrán használata a gyulladt vagy nyílt területek fedésére kedvezően befolyásolja a sebgyógyulási folyamatot, valamint csökkenti a beteg fájdalom- és kényelmetlenségi szintjét.3
A vastag magzatmembrán alkalmazásának pragmatikus szempontja, hogy könnyen alkalmazkodik a sebfelülethez, és akár ragasztással, akár varrással is rögzíthető a sebfelülethez. A membrán hidrofil, és természetes módon felszívja a környező folyadékokat. A gyógyulási folyamat részeként az amnionmembrán visszaszívódik a sebbe.
Az amnionmembrán alkalmazása a szemsebészetben
Az amnionmembránt széles körben használják a szemsebészetben biológiai kötésként a sérült szemszövet gyógyítására vagy pótlására. Vékony, könnyű, rugalmas és szinte átlátszó, így alkalmas a szem felszínén való alkalmazásra. Összevarrható vagy szövetragasztóval a helyére ragasztható. Az amnionmembránt kémiai égési sérülések, a szaruhártya vagy a kötőhártya fekélyeinek, pusztító fekélyeket okozó betegségek kezelésére és olyan sebészeti beavatkozások során használják, ahol szemszövetet kell eltávolítani.
Az alábbi példák három olyan szemészeti alkalmazást mutatnak be, ahol az amnionmembránt sikeresen használják.
1. példa: Steven Johnson-szindróma
Ez a bőr és a nyálkahártyák ritka, akut, hólyagosodó betegsége, amelyet gyógyszerek vagy fertőzések által kiváltott immunreakció okoz. A klinikai kép a részleges vastagságú égési sebekhez hasonló, és a szem érintettsége nagyon gyakori. A gyógyulás felgyorsítására és a fájdalom csillapítására sikeresen alkalmazzák az amnionmembránt.
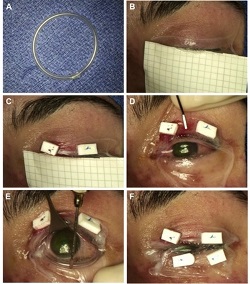
Példa 1. ábra: Magzatmembrán (AM) transzplantáció egyetlen 5 x10 cm-es lap felhasználásával. (A) Symblepheron-gyűrű létrehozása intravénás csővel. (B) Az AM elhelyezése a felső szemhéj fölé. (C) Az AM rögzítése 6-0 polipropilén matracvarratok és alátétek segítségével. (D) Az AM kibontása a szemfelszín felett. (E) Az egyedi készítésű symblepheron-gyűrű elhelyezése a fornicesben. A gyűrűt már betolták a felső fornixba, és óvatosan lerakják az alsó fornixba. (F) Az AM rögzítése az alsó szemhéjhoz.
A kép a következő forrásból származik: Ma K N , Thanos A, Chodosh J, Shah A S, Mantagos I S; A Novel Technique for Amniotic Membrane Transplantation in patients with Acute Stevens-Johnson Syndrome; The Ocular Surface, 2016; 14(1):31-36.
2. példa: Szaruhártya perforációk és fekélyek
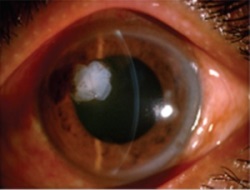
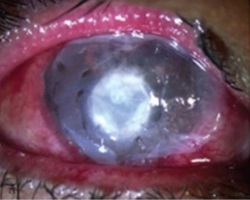
Ezek hatékonyan és gyorsan gyógyulnak, ha magzatmembránt használunk biológiai kötszerként az üreg kitöltésére.
2. példa Ábra: A szaruhártya perforáció műtéti lépései. Kisebb fekély és hirtelen szélű perforáció esetén egy tekercs magzatmembránt (AM) nyomunk a perforációba, és keresztöltéssel rögzítjük, ahogy a felső képen látható.
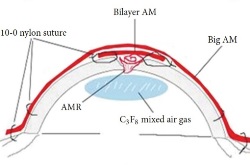
A középső képen látható nagyobb perforáció esetében először az AM-et tekercsbe hajtogattuk és bedugtuk a perforációba. Másodszor, a kétrétegű AM-et a tekercs és a fekély hámfelülettel felfelé fedte, és 10-0 nejlonvarratokkal rögzítették. Harmadszor, 0,3 ml 20%-os C3F8 (perfluor-propan) injekciót fecskendeztünk az elülső kamrába. Végül egy nagyobb AM-darabot helyeztek fel a teljes szaruhártyára ideiglenes tapaszként, és 2 körös 10-0 nejlonvarratokkal rögzítették a szaruhártya limbusához és a perilimbális episklerához.
Az alsó képen látható séma szemlélteti a magzatmembrán-tekercs, a kétrétegű magzatmembrán és a nagy magzatmembrándarab elhelyezését, amelyet a teljes szaruhártyára helyeztek.
A képek a következő forrásból származnak: Fan J, Wang M, Zhong F; Improvement of Amniotic Membrane Method for the Treatment of Corneal Perforation; BioMed Research International; 2016; Article ID 1693815.
Példa 3: Pterygium sebészet
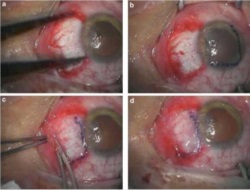
Az amnionmembránt sikeresen alkalmazzák ennél a gyakran végzett eljárásnál. A pterygium jóindulatú kinövés a szem kötőhártyáján, általában az orrhoz legközelebbi területen. Ezek a kinövések irritációt okozhatnak a szemben, és műtéti úton kell eltávolítani őket. Az eltávolítás után visszamaradt hiányt sikeresen gyógyítják az alább látható magzatmembrán-beültetéssel.
3. példa Ábra: A többrétegű magzatmembrán-graft műtéti eljárásai. (a) A pterygium kimetszése után a csupasz szklerális defektust kaliperrel mértük. (b) Az amnionmembránt gentian ibolyával jelölték meg, hogy biztosítsák a megfelelő méretű, a defektus területét fedő graftot. A membránt a szaruhártyára helyeztük úgy, hogy a hám/alaphártya oldala legyen felül. (c) A membránt a szklerális ágyra csúsztattuk, és a széleket sima csipesszel “összecsíptük” a recipiens kötőhártyával. (d) A membrán stabilitását cellulózszivaccsal ellenőriztük.
A képek a következő forrásból származnak: Fahmy RM; Pterygium Resection with Amniotic Membrane Grafting in a Patient with Xeroderma Pigmentosum; Austin J Clin Ophthalmol; 2016 Vol 3 (2); ISSN : 2381-9162
Az amnionmembrán ideális biológiai kötésnek bizonyult a szemészetben, és világszerte alkalmazzák. Tulajdonságai ideálisak a gyógyulás elősegítésére és kényelmet nyújtanak a betegnek.
Dr. Yvonne Holt a Next Biosciences orvosi igazgatója, egy dél-afrikai biotechnológiai vállalat, amely az orvostudományt, a tudományt és a technológiát kombinálja innovatív termékek és szolgáltatások létrehozása érdekében, lehetővé téve az emberek számára, hogy befektessenek és személyes felelősséget vállaljanak jövőbeli egészségükért. A Next Biosciences elsősorban a fogamzás előtti és a születés utáni piacokra összpontosít, és az újszülöttkori őssejtbankolásra, a genetikai vizsgálatokra, valamint az újszülöttkori szűrésre specializálódott. A Next Biosciencesnek van egy biológiai részlege is, amely méhlepényhártyából – a szemészeti sebészetben használt AmnioMatrix – és köldökzsinórvér-szérumból – OptiSerum szemcsepp – előállított terápiás termékeket fejleszt. Dr. Holt a Wits Egyetemen szerzett orvosi diplomát gyermekgyógyászatból és transzfúziós orvoslásból. Dr. Holt a [email protected]
- Perepelkin N, Hayward K, Mokeona T et al.; Cryopreserved amniotic membrane as a transplant allograft: viability and post-transplant outcome; Cell and Tissue Banking 2016; 17(1):39-50.
- Rahman I, Said DG, Maharajan VS, Dua HS. Magzatmembrán a szemészetben: indikációk és korlátok. Eye. 2009; 23(10):1954-61.
- Dua HS, Gomes JA., King AJ, Maharajan VS. A magzatmembrán a szemészetben. Survey of Ophthalmology. 2004; 49(1):51-77.
- Niknejad H, Peirovi H, Jorjani M, Ahmadiani A, Ghanavi J, Seifalian AM. Az amnionmembrán tulajdonságai a szövettechnológiában való potenciális felhasználás szempontjából. European Cells and Matererials. 2008; 15:88-99.
- Tyszkiewicz JT, Uhrynowska-Tyszkiewicz IA, Kaminski A, Dziedzic-Goclawska A. A varsói Központi Szövetbankban készített amnion allograftok. Annals of transplantation: a Lengyel Transzplantációs Társaság negyedéves száma. 1999; 4(3-4):85.
- Bourne G. The Fœtal Membranes. A normális Amnion és Chorion anatómiájának és működésük néhány szempontjának áttekintése. Postgrad Med J. 1962; 38(438):193-201.
- Jiang A, Li C, Gao Y, Zhang M, Hu J, Kuang W, et al. In vivo and in vitro inhibitory effect of amniotic extraction on neovascularization. Cornea. 2006; 25:S36-S40.