Nézze meg a legújabb cikkeket
A 27 éves, atheroscleroticus kardiovaszkuláris betegséggel és távoli myocardialis infarktussal, asztmával és provokált mélyvénás trombózissal (befejezett antikoagulációval) rendelkező nő két napja súlyosbodó mellkasi fájdalom és nehézlégzés panaszaival jelentkezett. Tagadta a lázat, hidegrázást, produktív köhögést vagy a beteggel való érintkezést. Beismerte, hogy 7 hónap alatt 70 fontot fogyott akaratlanul, csökkent az étvágya, éjszakai izzadás, hasmenés és szívdobogás.
Az életjelek szerint a pulzusszám 95, a vérnyomás 113/74 mmHg, a légzésszám 14, a SpO2 95% szobai levegőn. Az átfogó metabolikus panel és a teljes vérkép normális volt. Az EKG normális szinuszritmust mutatott, bal kamrai hipertrófiával és ST-változás nélkül. A vizelet drogszűrés csak kannabinoidra volt pozitív. A szívmarkerek negatívak voltak. A TSH 0,01 mclU/mL volt (0,31-5,00 mclU/mL).
Kórházi 1. nap: A mellkasröntgen a jobb felső tüdő fölött a 3. elülső és a 6. hátsó borda metszéspontjánál egy kis sűrűséget mutatott. A tüdő CT angiográfiás követése meghatározhatatlan homogén tömör tömeget mutatott ki az elülső felső mediastinumban az aortaív mentén, melynek mérete kb. 5,5 cm x 5,3 cm x 2,4 cm craniocaudalis, keresztirányú és AP méretekben. A tömeg nem volt folytonos a pajzsmiriggyel, és nem mutatott cisztás vagy meszes komponenst. A CT-képalkotó vizsgálaton fokális elváltozás nélküli pajzsmirigy-megnagyobbodást észleltek. A szív normális méretű volt, perikardiális folyadékgyülem és összeesett alsó véna cava nélkül. Az US pajzsmirigy kétoldali thyromegáliát mutatott hypervascularitással és diszkrét gócok nélkül.
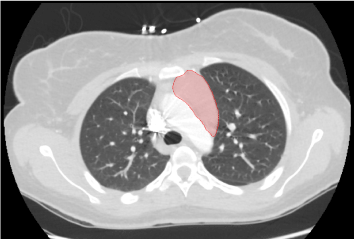
1. ábra . Közepes homogén tömör tömeg a felső mediastinumban, mérete 5,5 cm x 5,3 cm x 2,4 cm.
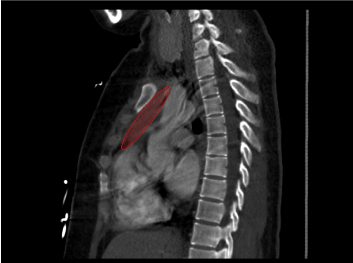
2. ábra. A tömeg ábrázolása sagittalis nézetben.
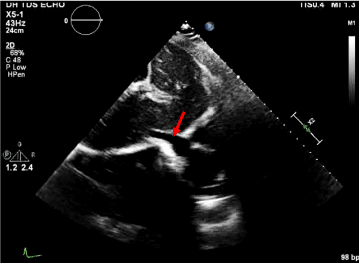
3. ábra. Összeomló IVC pericardialis folyadékgyülem jelei nélkül.
Kórházi 2. nap: Az esetleges lymphoma vagy thymoma gyanúja miatt az intervenciós radiológiát és az onkológiát keresték fel, hogy további értékelés céljából biopsziát vegyenek az elülső mediastinalis tömegből.
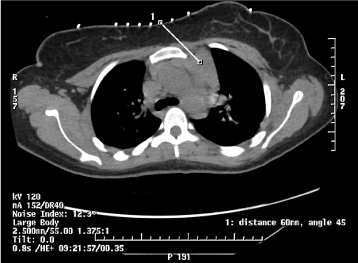
4. ábra. CT-vezérelt 18-as magbiopszia a bal elülső felső mediastinumban lévő kóros lágyrészsűrűség felvételére.
Röviddel a mediastinalis tömeg CT-vezérelt tűbiopsziájáról való visszatérés után a betegnél hányinger, heves hányás jelentkezett, és nem reagált. A gyorsreagálású csapat megérkezésekor az életjelek a következők voltak: pulzusszám 150, vérnyomás 65/50 mmHg, RR 20, SpO2 95% 6 l oxigén mellett. Az EKG szinuszos tachikardiát mutatott ST-változás nélkül. A betegnek 1 liter normál sóoldatot adtak, és sürgősséggel csomagolt vörösvértesteket készítettek elő, mivel a biopszia szövődményeként tüdőartéria-sérüléstől tartottak. Az ágy melletti ultrahang perikardiális folyadékgyülemet, nem összenyomható alsó vena cavát és kamrai interdependenciát mutatott, ami a tamponád fiziológiáját mutatja. A beteget intubálták a légutak védelmére, és sürgősen konzultáltak a szív- és mellkassebészettel a perikardiocentézis és a feltételezett mediastinalis hematóma eltávolítása céljából. A mellkasröntgen megerősítette a mediastinalis vérömlenyre gyanús jelentős mediastinalis kiszélesedést .
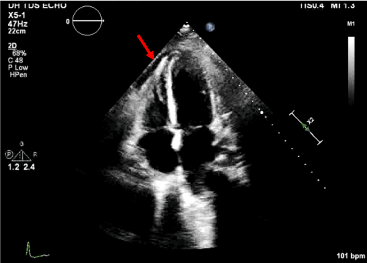
5. ábra. Axiális 4 kamrás felvétel perikardiális folyadékgyülemmel.
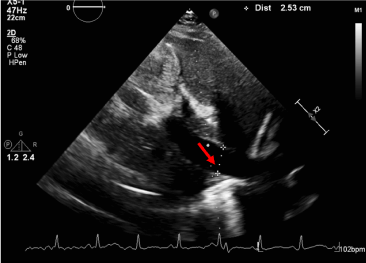
6. ábra. Nem összenyomható alsó vena cava inferior. A tágult IVC jelenléte 50%-nál kisebb mértékű összeomlással erőltetett belégzéskor korrelál az emelkedett centrális vénás nyomással és megerősíti a tamponád fiziológiáját.
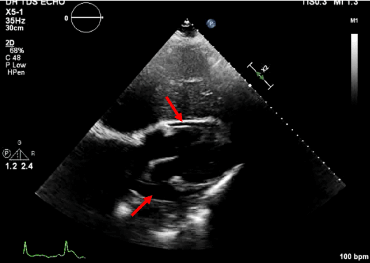
7. ábra. Subcostalis nézet perikardiális folyadékgyülemmel.
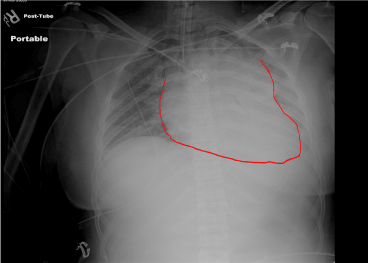
8. ábra. Intubáció utáni röntgenfelvétel. Endotrachealis tubus a helyén. Mediastinalis hematoma gyanúja miatt kiszélesedett mediastinum.
A laboratóriumi vizsgálatok áttekintése a beteg intenzív osztályra szállítását követően TSH 0,01 mclU/mL (0,31-5,00 mclU/mL), reflexes szabad T4 > 4,2 ng/dl (0,7-1,7 ng/dl) és T3 > 651 (71-170ng/dl). Az acetilkolinreceptor-kötő antitest negatív volt. Burch-Wartofsky pontszám > 45, ami a pácienst pajzsmirigystormának minősítette.
Elkerülhetetlen feltáró median szternotómiát végeztek propiltiuracil, hidrokortizon-nátrium-szukcinát és lugol-jódoldat intraoperatív beadásával. A mediastinalis feltárás nagyméretű elülső mediastinalis tömeget tárt fel vérzéssel, amelyet eltávolítottak. A szívburok falának behatolására utaló jeleket észleltek; 150 cm3 vért és vérrögöt ürítettek ki. Egyenes mellkasi csöveket helyeztek mindkét mellhártyaüregbe. A beteget stabil állapotban visszaszállították az intenzív osztályra.
A mediastinalis anterior tömeg patológiai vizsgálata egy 90,8 gramm súlyú, kétoldali tímuszmirigyet azonosított. A mediastinalis tömeg szöveti biopsziájának szövettani elemzése jóindulatú thymus hyperplasiát mutatott ki, amely valószínűleg a kezeletlen hyperthyreosis következménye.
A beteget stabil állapotban hazaengedték propranolol, propylthiouracil és az endokrinológus követésére vonatkozó utasítás mellett.
Diszkusszió
A képvezérelt mediastinalis biopszia általában biztonságos és minimálisan invazív eljárás. Többféle megközelítés és sokféle képalkotó technika létezik – az ultrahang és a komputertomográfia (CT) által vezérelt módszerek a leggyakoribbak. A képalkotó technikát bizonyos jellemzők alapján választják ki: klinikai körülmények, a tömeg elhelyezkedése, a tömeg mérete és a biopsziával vizsgált minta alapbetegségei. A megközelítés kiválasztása előtt figyelembe veszik az anatómiai és technikai szempontokat, az érrendszeri komponenseket/élettani szerveket, a tűk kiválasztását és a patológiai megfontolásokat.
A közvetlen mediastinalis megközelítések közé tartoznak a para-vertebralis, a suprasternalis, a trans-pulmonalis és az extra pleurális megközelítések. A CT-vezérelt perkután biopsziának számos előnye van más alternatív technikákkal szemben. Lehetővé teszi a céllézió pontos lokalizációját és a mediastinalis rekeszekhez való hozzáférést, amelyek mediastinoscopiával vagy endobronchiális biopsziával nem könnyen hozzáférhetőek. Az USA-vezérelt perkután biopszia a CT-vezérelthez képest rendelkezik néhány előnnyel, különösen azzal, hogy valós időben végezhető, a tű folyamatos megfigyelésével a tű előrehaladása és a mintavétel során. Az US-vezérléssel több ferde útvonal is könnyen elérhető, és hordozhatósága lehetővé teszi a kritikus állapotú betegek ágy melletti biopsziájának elvégzését .
A CT-vezérelt biopszia részletes képalkotást és többsíkú reformációkat biztosít, amelyek segítenek elkerülni a mellüregben lévő érrendszeri struktúrák és létfontosságú szervek szúrását. A CT-vezérelt perkután transtorakális tűbiopszia kevésbé invazív, mint a mediastinoszkópia, és csak helyi érzéstelenítést igényel. A perkután transthoracalis tűbiopszia alkalmazásának kevés ellenjavallata a hidatidaciszta gyanúja (abszolút ellenjavallat), a koagulopátia és a súlyosan károsodott tüdőfunkció, beleértve a bullous emphysemát, a pulmonális hipertóniát vagy az érdaganatot.
Betegünknél a bal parasternalis és retrosternalis régióban elhelyezkedő anterior mediastinalis tömeget azonosítottak. Elülső vagy középső mediastinalis tömeg esetén, ha a betegnek nincs ellenjavallata, leggyakrabban a parasternalis megközelítést alkalmazzák CT-vezérléssel. A paraszternális megközelítés során a tűt a paraszternális izmokon és a mediastinalis zsírszöveten keresztül vezetik be a céllézióba. A tű előrehaladása között több felvétel készül a pálya ellenőrzésére, hogy a belső emlőerek ne kerüljenek útjába. Egy 22-es tűvel sóoldatot vagy hígított kontrasztanyagot lehet befecskendezni a mediastinum kiszélesítésére és a tű behelyezéséhez mesterséges extrapleurális útvonal létrehozására. A biztonságos extrapleurális ablak létrehozása után a 22-es tűt eltávolítják, és egy nagy furatú (18-as vagy nagyobb) vezető tűt vezetnek be. A koaxiális technika alkalmazásával a finom tűs aspiráció és a magbiopszia a vezető tűn keresztül történik .
A mediastinalis biopsziák gyakori szövődményei közé tartoznak a vasovagális reakciók, a légembólia és a tumor elszaporodása . A CT-vezérelt mediastinalis tömegbiopszia súlyos szövődményei szokatlanok, és a halálesetek nagyon ritkák . A mediastinalis biopszia leggyakoribb életveszélyes szövődménye a pneumothorax, amelynek előfordulása 27%-54% között mozog a biopszia után . Egy nagy retrospektív sorozat szerint a pneumothorax előfordulása 20,5%, a mellkasi drénezést igénylő pneumothorax előfordulása pedig 3,1% . Egyéb szövődmények közé tartozik a tüdővérzés hemoptízissel vagy anélkül, hemothorax és mellkasfalvérzés . Hemothorax esetén az akut fázisban mellkascső-drenázs javasolt, amelyet a szubakut fázisban lytikus terápia követ. Weinberg és munkatársai 2006-2011 között összesen 830 mellkasi biopsziát tekintettek át, és megállapították, hogy 830-ból összesen 4 esetben (0,5%) alakult ki biopszia utáni hemothorax, 33-71 év közötti életkorban. A betegek egyike sem mutatott kóros véralvadási értékeket vagy vérlemezkeszámot, és megjegyzendő, hogy egy betegnél a tünetek több mint 12 órával később jelentkeztek. Tomiyama és munkatársai egy japán kórházakban végzett felmérés során megállapították, hogy a perkután tüdőbiopsziáknak csak 0,092%-a vezetett hemothoraxhoz . Yeowet és munkatársai 680 koaxiális biopszia közül csak 1 esetben (0,2%) jelentettek hemothorax szövődményt .
Vérzésről számoltak be, amely tüdőforrásból vagy bordaközi artéria sérüléséből eredt. Egyetlen esetben sem számoltak be szívtamponádot eredményező szívburok-sérülésről.
A mi esetünkben a betegnél hemoperikardiumból eredő szívtamponád alakult ki, ami a mediastinalis biopsziák ritkán jelentett szövődménye . Feltételezzük, hogy esetünkben a tű kis szakadást képzett a tüdőérben, és a szövetkivétel során kommunikációt okozott a tüdőartéria és a perikardium között. Szerencsére a diagnózist gyorsan sikerült felállítani, és a beteget sürgősségi feltáró median sternotomiára vitték.
Következtetés
A képvezérelt perkután biopsziát rutinszerűen alkalmazzák a mediastinalis elváltozások diagnosztizálására. A céllézió pontos lokalizációjához komputertomográfiát (CT) és ultrahangos irányítást használnak. A CT-képalkotás a legjobb képalkotó módszernek bizonyult a tűbiopszia irányításához . A megfelelő megközelítés eldöntésében szerepet játszó tényezők közé tartoznak a klinikai körülmények, a céllézió elhelyezkedése, mérete és a társbetegségek . A perkután biopszia legjobb megközelítését a korábbi felvételek és a kórtörténet áttekintésével kell meghatározni. Feltétlenül fel kell ismerni, hogy a szövődmények kockázata a megközelítés típusától függően változhat. A magas diagnosztikai pontosság és a szövődmények ritka előfordulása ellenére feltétlenül meg kell határozni a legbiztonságosabb hozzáférést, és éberen kell figyelni minden szövődményre, és indikáció esetén azonnali kezelést kell biztosítani.
- Gupta S, Seaberg K, Wallace M (2005) Imaging-guided percutan biopsy of mediastinal lesions: different approaches and anatomic considerations. Radiographics 25: 763-786.
- Kulkarni S, Kulkarni A, Roy D, Thakur MH (2008) Perkutan komputertomográfiával irányított magbiopszia a mediastinalis tömegek diagnosztikájában. Annals of Thoracic Medicine 3: 13-17.
- Westcott JL (1988) Percutan transthoracalis tűbiopszia. Radiology 169: 593-601.
- Langen HJ, Klose KC, Keulers P, Adam G, Jochims M, Gunther RW (1995) Artificial widening of the mediastinum to gain access for extrapleural biopsy: clinical results. Radiology 196: 703-706.
- Hira L, Neyaz Z, Nath A, Borah S (2012) CT-vezérelt perkután biopszia intrathoracalis elváltozásoknál. Korean J Radiol 13: 210-226.
- Bressler EL, Kirkham JA (1994) Mediasztinális tömegek: A CT-vezérelt tűbiopszia alternatív megközelítései. Radiology 191: 391-396.
- Richardson CM, Pointon KS, Manhire AR, Macfarlane JT (2002) Perkutan tüdőbiopszia: az Egyesült Királyság gyakorlatának felmérése 5444 biopszia alapján. Br J Radiol 75: 731-735.
- Weinberg, B, Watumull, L, Landay M, Omar, H (2013) Variable presentations of thoracic biopsy related hemothorac. Universal Journal of Clinical Medicine 1: 22-27.
- Tomiyama N, Yasuhara Y, Nakajima Y, Adachi S, Arai Y, Kusumoto M, et al. (2006) CT-guided needle biopsy of lung lesions: a survey of severe complication based on 9783 biopsies in Japan. European Journal of Radiology 59: 60-64.
- Protopapas Z, Westcott JL (2000) Transthoracalis hilaris és mediastinalis biopszia. Radiol Clin North Am 38: 281-289.