Alfenta
Generieke naam: Alfentanilhydrochloride
Doseringsvorm: injectie
Medisch beoordeeld door Drugs.com. Laatst bijgewerkt op 22 jan 2021.
- Bijwerkingen
- Dosering
- Professional
- Interacties
- Zwangerschap
- Meer
CII
Rx only
- Alfenta Beschrijving
- Alfenta – Klinische Farmacologie
- Indicaties en gebruik voor Alfenta
- Contra-indicaties
- Waarschuwingen
- Voorzorgsmaatregelen
- Algemeen
- Hoofdletsel
- Geperkte ademhaling
- Geperkte lever- of nierfunctie
- Gedragsinteracties
- Carcinogenese, mutagenese en aantasting van de vruchtbaarheid
- Volwassenheid Categorie C
- Labor and Delivery
- Verloskundige moeders
- Pediatrisch gebruik
- Bijwerkingen
- Incidentie groter dan 1% – Waarschijnlijk oorzakelijk verband (Afgeleid van klinische onderzoeken)
- Incidentie Minder dan 1% – Waarschijnlijk Oorzakelijk verband (Afgeleid van klinische proeven)
- Drugsgebruik en -afhankelijkheid
- Overdosering
- Alfenta dosering en toediening
- Gebruik bij kinderen
- Premedicatie
- Neuromusculaire blokkeringsmiddelen
- Veiligheid EN BEHANDELING
- Hoe wordt Alfenta geleverd
Alfenta Beschrijving
Alfenta (Alfentanilhydrochloride) Injectie is een opioïd pijnstillend middel chemisch aangeduid als N–4-(methoxymethyl)-4-piperidinyl]-N-fenylpropanamide monohydrochloride (1:1) met een molecuulgewicht van 452.98 en een n-octanol:water verdelingscoëfficiënt van 128:1 bij pH 7,4. De structuurformule van Alfenta is:
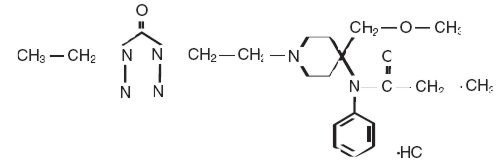
Alfenta is een steriele, niet pyrogene, conserveermiddelvrije waterige oplossing die Alfentanilhydrochloride bevat, overeenkomend met 500 µg per ml Alfentanil-base voor intraveneuze injectie. De oplossing, die natriumchloride bevat voor isotoniciteit, heeft een pH-bereik van 4-6. Elke ml bevat: Actief: Alfentanil base 500 mcg. Inactief: Natriumchloride 9 mg en Water voor Injectie Q.S.
Alfenta – Klinische Farmacologie
Alfenta (Alfentanilhydrochloride) is een opioïd pijnstillend middel met een snel begin van werking.
Bij doses van 8-40 mcg/kg voor chirurgische ingrepen die tot 30 minuten duren, biedt Alfenta analgetische bescherming tegen hemodynamische reacties op chirurgische belasting met hersteltijden die in het algemeen vergelijkbaar zijn met die van fentanyl in gelijke doses.
Bij langere ingrepen verminderen doses tot 75 mcg/kg de hemodynamische reacties op laryngoscopie, intubatie en incisie, met hersteltijden die vergelijkbaar zijn met die van fentanyl. Bij doses van 50-75 mcg/kg gevolgd door een continue infusie van 0,5-3 mcg/kg/min, dempt Alfenta de catecholaminereactie met een sneller herstel en minder behoefte aan postoperatieve analgetica in vergelijking met patiënten die enfluraan toegediend krijgen. Bij doses van 5 mcg/kg geeft Alfenta analgesie aan de bewuste maar gesedeerde patiënt. Op basis van de respons van de patiënt kunnen hogere doses dan 5 mcg/kg nodig zijn. Oudere of verzwakte patiënten kunnen lagere doses nodig hebben. De farmacokinetiek van Alfenta kan worden beschreven als een drie-compartimentenmodel met sequentiële distributiehalfwaardetijden van 1 en 14 minuten; en een terminale eliminatiehalfwaardetijd van 90-111 minuten (in vergelijking met een terminale eliminatiehalfwaardetijd van ongeveer 475 minuten voor fentanyl en ongeveer 265 minuten voor sufentanil bij doses van 250 mcg). De lever is de belangrijkste plaats van biotransformatie.
Alfenta heeft een schijnbaar verdelingsvolume van 0,4-1 L/kg, wat ongeveer eenvierde tot een tiende is van dat van fentanyl, met een gemiddelde plasmaklaring van 5 ml/kg/min in vergelijking met ongeveer 8 ml/kg/min voor fentanyl.
Slechts 1,0% van de dosis wordt als onveranderd geneesmiddel uitgescheiden; urinaire excretie is de belangrijkste eliminatieroute van metabolieten. De plasma-eiwitbinding van Alfenta is ongeveer 92%.
In één onderzoek met 15 patiënten die Alfenta toegediend kregen met lachgas/zuurstof, bleek een smal bereik van plasma Alfenta concentraties, ongeveer 310-340 ng/mL, adequate anesthesie te verschaffen voor intra-abdominale chirurgie, terwijl lagere concentraties, ongeveer 190 ng/mL, reacties op het sluiten van de huid blokkeerden. Plasmaconcentraties tussen 100-200 ng/mL gaven adequate anesthesie voor oppervlakkige chirurgie.
Alfenta heeft een onmiddellijk begin van werking. Bij doseringen van ongeveer 105 mcg/kg veroorzaakt Alfenta hypnose zoals bepaald door EEG-patronen; een anesthesie ED90 van 182 mcg/kg voor Alfenta bij patiënten zonder medicatie is vastgesteld, gebaseerd op het vermogen om de reactie op het plaatsen van een nasofaryngeale luchtweg te blokkeren. Op basis van klinisch onderzoek varieert de vereiste inductiedosis van 130-245 mcg/kg. Voor procedures die 30-60 minuten duren, geven laaddoses tot 50 mcg/kg een hemodynamische respons op endotracheale intubatie en huidincisie die vergelijkbaar is met die van fentanyl. Een pre-intubatie laaddosis van 50-75 mcg/kg voorafgaand aan een continue infusie vermindert de reactie op laryngoscopie, intubatie en incisie. De daaropvolgende toediening van een Alfenta infuus met een snelheid van 0,5-3 mcg/kg/min met lachgas/zuurstof vermindert de sympathische reacties op chirurgische stress met een sneller herstel dan enfluraan.
De behoefte aan vluchtige inhalatieanesthetica werd gedurende de eerste 60 minuten met dertig tot vijftig procent verminderd bij patiënten die een verdovingsdosis (meer dan 130 mcg/kg) Alfenta toegediend kregen, vergeleken met patiënten die een dosis van 4-5 mg/kg thiopental toegediend kregen voor anesthesie-inductie. Bij anesthesie-inductiedoses zorgt Alfenta voor een diep niveau van anesthesie tijdens het eerste uur van anesthesie-onderhoud en voor demping van de hemodynamische respons tijdens intubatie en incisie.
Na een anesthesie-inductiedosis Alfenta wordt de behoefte aan Alfenta-infusie tijdens het eerste uur van onderhoud met 30 tot 50% verminderd.
Patiënten met een gecompromitteerde leverfunctie en personen ouder dan 65 jaar blijken een verminderde plasmaklaring en een verlengde terminale eliminatie voor Alfenta te hebben, wat het postoperatieve herstel kan verlengen. Herhaalde of voortdurende toediening van Alfenta leidt tot stijgende plasmaconcentraties en een accumulatie van het geneesmiddel, vooral bij patiënten met een verminderde plasmaklaring.
Bradycardie kan worden waargenomen bij patiënten die Alfenta toegediend krijgen. De incidentie en de graad van bradycardie kunnen meer uitgesproken zijn wanneer Alfenta wordt toegediend samen met niet-vagolytische neuromusculaire blokkeringsmiddelen of in afwezigheid van anticholinerge middelen zoals atropine.
Toediening van intraveneuze diazepam onmiddellijk voorafgaand aan of volgend op hoge doses Alfenta is aangetoond dat dit verlagingen van de bloeddruk veroorzaakt die secundair kunnen zijn aan vasodilatatie; het herstel kan ook worden verlengd.
Patiënten die doses tot 200 mcg/kg Alfenta toegediend kregen, vertoonden geen significante verhoging van de histamine-spiegels en geen klinisch bewijs van histamine-afgifte.
Skeletspierrigiditeit is gerelateerd aan de dosis en de snelheid van toediening van Alfenta. Spierstijfheid zal optreden met een onmiddellijk begin na anesthesie-inductiedoseringen. Preventieve maatregelen (zie WAARSCHUWINGEN) kunnen de snelheid en de ernst verminderen.
De duur en de mate van ademhalingsdepressie en verhoogde luchtwegweerstand nemen gewoonlijk toe met de dosis, maar zijn ook waargenomen bij lagere doses. Hoewel hogere doses apneu en een langere duur van ademhalingsdepressie kunnen veroorzaken, kan apneu ook bij lage doses voorkomen.
Tijdens gemonitorde anesthesiezorg (MAC) moet aandacht worden besteed aan de ademhalingseffecten van Alfenta Injectie. Verlaagde zuurstofsaturatie, apneu, verlaagde ademhalingsfrequentie en obstructie van de bovenste luchtwegen kunnen optreden. (Zie WAARSCHUWINGEN)
Indicaties en gebruik voor Alfenta
Alfenta (Alfentanilhydrochloride) is geïndiceerd:
als een analgetisch adjunct dat in stapsgewijze doses wordt toegediend bij het handhaven van anesthesie met barbituraat/nitrous oxide/zuurstof. als analgeticum toegediend via continue infusie met lachgas/zuurstof bij de handhaving van de algehele anesthesie. als primair anestheticum voor de inductie van anesthesie bij patiënten die algehele chirurgie ondergaan waarbij endotracheale intubatie en mechanische beademing vereist zijn. als analgetisch bestanddeel voor gemonitorde anesthesiezorg (MAC).
Zie de doseringskaart voor uitgebreidere informatie over het gebruik van Alfenta.
Contra-indicaties
Alfenta (Alfentanilhydrochloride) is gecontra-indiceerd bij patiënten met bekende overgevoeligheid voor het geneesmiddel of bekende intolerantie voor andere opioïde agonisten.
Waarschuwingen
Alfenta DIENT ALLEEN TE WORDEN TOEGEEDIEN DOOR PERSONEN die SPECIFIEK OPgeleid zijn IN HET GEBRUIK VAN INTRAVENE EN ALGEMENE ANESTHETISCHE AGENTIA EN IN HET BEHEER VAN DE RESPIRATORISCHE EFFECTEN VAN POTENT OPIOIDS.
EEN OPIOÏD-ANTAGONIST, REANIMATIE- EN INTUBATIEAPPARATUUR EN ZUURSTOF MOETEN DIRECT BESCHIKBAAR ZIJN.
WEGENS DE MOGELIJKHEID VAN VERTRAAGDE ADEMHALINGSDEPRESSIE MOET DE BEWAKING VAN DE PATIËNT TOT LANG NA DE OPERATIE WORDEN VOORTGEZET.
Alfenta (Alfentanilhydrochloride) toegediend in initiële doseringen tot 20 mcg/kg kan stijfheid van de skeletspieren veroorzaken, met name van de truncale spieren. De incidentie en de ernst van spierstijfheid is gewoonlijk dosisgerelateerd. Toediening van Alfenta in inductiedoseringen voor anesthesie (meer dan 130 mcg/kg) zal consequent spierstijfheid veroorzaken met een onmiddellijk begin. Het begin van spierstijfheid treedt eerder op dan bij andere opioïden. Alfenta kan spierstijfheid veroorzaken waarbij alle skeletspieren betrokken zijn, inclusief die van de nek en de ledematen. De incidentie kan worden verminderd door: 1) routinemethoden voor de toediening van neuromusculaire blokkeringsmiddelen voor evenwichtige opioïdenanesthesie; 2) toediening van maximaal 1/4 van de volledige verlammende dosis van een neuromusculair blokkeringsmiddel vlak voor de toediening van Alfenta in doseringen tot 130 mcg/kg; na het verlies van het bewustzijn moet een volledige verlammende dosis van een neuromusculaire blokker worden toegediend; of 3) gelijktijdige toediening van Alfenta en een volledige verlammende dosis van een neuromusculaire blokker wanneer Alfenta wordt gebruikt in snel toegediende doses anesthesie (meer dan 130 mcg/kg).
Het gebruikte neuromusculaire blokkeringsmiddel dient geschikt te zijn voor de cardiovasculaire status van de patiënt. Er moeten adequate voorzieningen beschikbaar zijn voor postoperatieve bewaking en beademing van patiënten die Alfenta toegediend krijgen. Het is van essentieel belang dat deze faciliteiten volledig zijn uitgerust om alle gradaties van ademhalingsdepressie aan te kunnen.
PATIËNTEN DIE BEWAAKTE ANESTHESIEZORG (MAC) KRIJGEN, MOETEN VOORTDUREND WORDEN BEWAAKT DOOR PERSONEN DIE NIET BETROKKEN ZIJN BIJ DE UITVOERING VAN DE CHIRURGISCHE OF DIAGNOSTISCHE PROCEDURE; ZUURSTOFSUPPLETIE MOET ONMIDDELLIJK BESCHIKBAAR ZIJN EN WORDEN VERSTREKT WAAR DIT KLINISCH GEÏNDICEERD IS; DE ZUURSTOFSATURATIE MOET VOORTDUREND WORDEN BEWAAKT; DE PATIËNT MOET WORDEN GEOBSERVEERD OP VROEGE TEKENEN VAN HYPOTENSIE, APNEU, OBSTRUCTIE VAN DE BOVENSTE LUCHTWEGEN EN/OF ZUURSTOFDESATURATIE.
Severe en onvoorspelbare potentiëring van monoamine oxidase (MAO) remmers is gemeld voor andere opioïde analgetica, en zelden met Alfentanil. Wanneer Alfentanil wordt toegediend aan patiënten die binnen 14 dagen MAO-remmers hebben gekregen, wordt daarom adequate monitoring en de onmiddellijke beschikbaarheid van vasodilatoren en bètablokkers voor de behandeling van hypertensie aanbevolen.
Voorzorgsmaatregelen
GEDELATEERDE REPIRATORISCHE DEPRESSIE, REPIRATORISCHE ARREST, BRADYCARDIA, ASYSTOLIE, ARRHYTHMIAS EN HYPOTENSIE HEBBEN OOK GERAPPORTEERD. Daarom moeten de vitale symptomen voortdurend worden gecontroleerd.
Algemeen
De aanvangsdosis Alfenta (Alfentanilhydrochloride) moet bij oudere en verzwakte patiënten op gepaste wijze worden verlaagd. Het effect van de initiële dosis dient in overweging te worden genomen bij het bepalen van aanvullende doses. Bij obese patiënten (meer dan 20% boven het ideale totale lichaamsgewicht) moet de dosering van Alfenta worden bepaald op basis van het magere lichaamsgewicht.
In één klinisch onderzoek was de dosis Alfenta die nodig was om anesthesie te produceren, zoals bepaald door het verschijnen van delta-golven in het EEG, 40% lager bij geriatrische patiënten dan de dosis die nodig was bij gezonde jonge patiënten.
Bij patiënten met een gecompromitteerde leverfunctie en bij geriatrische patiënten kan de plasmaklaring van Alfenta verminderd zijn en kan het postoperatieve herstel langer duren.
Inductiedoses Alfenta dienen langzaam (langer dan drie minuten) te worden toegediend. Toediening kan verlies van vasculaire tonus en hypotensie veroorzaken. Vochtvervanging voorafgaand aan inductie dient te worden overwogen.
Diazepam toegediend onmiddellijk voorafgaand aan of in combinatie met hoge doses Alfenta kan vasodilatatie en hypotensie veroorzaken en resulteren in vertraagd herstel.
Bradycardie veroorzaakt door Alfenta kan worden behandeld met atropine. Ernstige bradycardie en asystolie zijn met succes behandeld met atropine en conventionele reanimatiemethoden.
Bij de keuze van een neuromusculair blokkeringsmiddel moet rekening worden gehouden met de hemodynamische effecten van een bepaald spierverslappend middel en met de vereiste mate van ontspanning van de skeletspieren.
Na een anesthesie-inductiedosis Alfenta worden de vereisten voor vluchtige inhalatieanesthetica of Alfenta-infusie gedurende het eerste uur van onderhoud met 30 tot 50% verminderd.
Alfenta-infusies moeten ten minste 10-15 minuten voor het einde van de operatie tijdens algehele anesthesie worden gestaakt. Tijdens toediening van Alfenta voor bewaakte anesthesiezorg (MAC) mogen infusies worden voortgezet tot het einde van de procedure.
Respiratoire depressie veroorzaakt door opioïde analgetica kan worden omgekeerd door opioïde antagonisten zoals naloxon. Omdat de duur van de door Alfenta veroorzaakte ademhalingsdepressie langer kan duren dan de duur van de werking van de opioïde-antagonist, moet de nodige waakzaamheid worden betracht. Zoals met alle krachtige opioïden gaat diepe analgesie gepaard met ademhalingsdepressie en verminderde gevoeligheid voor CO2-stimulatie, die kunnen aanhouden of terugkeren in de postoperatieve periode. Intraoperatieve hyperventilatie kan de postoperatieve reactie op CO2 verder veranderen. Passende postoperatieve bewaking dient te worden toegepast, met name na infusies en grote doses Alfenta, om ervoor te zorgen dat adequate spontane ademhaling wordt vastgesteld en gehandhaafd in afwezigheid van stimulatie alvorens de patiënt uit de verkoeverruimte te ontslaan.
Hoofdletsel
Alfenta dient met voorzichtigheid te worden gebruikt bij patiënten met hoofdletsel of verhoogde intracraniële druk, vanwege het verhoogde risico op ademhalingsdepressie. Zoals met alle opioïden kan Alfenta het klinisch beloop van patiënten met hoofdletsel vertroebelen en dient alleen te worden gebruikt indien klinisch geïndiceerd.
Geperkte ademhaling
Alfenta dient met voorzichtigheid te worden gebruikt bij patiënten met een longaandoening, verminderde ademhalingsreserve of een mogelijk gecompromitteerde ademhaling. Bij dergelijke patiënten kunnen opioïden bovendien de ademhalingsdrang verminderen en de luchtwegweerstand verhogen. Tijdens de anesthesie kan dit worden beheerst door geassisteerde of gecontroleerde ademhaling.
Geperkte lever- of nierfunctie
Bij patiënten met lever- of nierfunctiestoornissen dient Alfenta met voorzichtigheid te worden toegediend vanwege het belang van deze organen bij het metabolisme en de excretie van Alfenta.
Gedragsinteracties
Zowel de omvang als de duur van de effecten op het centrale zenuwstelsel en de cardiovasculaire effecten kunnen worden versterkt wanneer Alfenta wordt toegediend in combinatie met andere CNS-depressiva zoals barbituraten, kalmeringsmiddelen, opioïden of algemene inhalatieanesthetica. De postoperatieve ademhalingsdepressie kan door deze middelen worden versterkt of verlengd. In dergelijke gevallen van gecombineerde behandeling moet de dosis van één of beide middelen worden verlaagd. Uit beperkte klinische ervaring blijkt dat de behoefte aan vluchtige inhalatieanesthetica gedurende de eerste zestig (60) minuten na inductie met Alfenta met 30 tot 50% wordt verminderd.
Het gelijktijdig gebruik van erytromycine met Alfenta kan de klaring van Alfenta aanzienlijk remmen en kan het risico op verlengde of vertraagde ademhalingsdepressie verhogen.
Cimetidine vermindert de klaring van Alfenta. Daarom zullen bij langdurige toediening kleinere Alfenta-doses nodig zijn en kan de werkingsduur van Alfenta worden verlengd.
Perioperatieve toediening van geneesmiddelen die de leverdoorbloeding of enzymactiviteit beïnvloeden, kan de plasmaklaring verminderen en het herstel verlengen.
Carcinogenese, mutagenese en aantasting van de vruchtbaarheid
Er zijn geen langetermijnstudies met dieren naar Alfenta uitgevoerd om het carcinogene potentieel te beoordelen. Er werden geen structurele chromosoommutaties veroorzaakt bij de in vivo micronucleustest bij vrouwelijke ratten bij eenmalige intraveneuze doses van Alfenta tot 20 mg/kg lichaamsgewicht (ongeveer 40 keer de hoogste menselijke dosis), wat overeenkomt met een dosis van 103 mg/m2 lichaamsoppervlak. Er werden geen dominante letale mutaties veroorzaakt bij de in vivo dominante letale test bij mannelijke en vrouwelijke muizen bij de maximale intraveneuze dosis van 20 mg/kg (60 mg/m2 ). Er werd geen mutagene activiteit aangetoond in de in vitro Ames Salmonella typhimurium-test, met en zonder metabole activering.
Volwassenheid Categorie C
Alfenta heeft bij ratten en konijnen een embryocidaal effect aangetoond wanneer het gedurende een periode van 10 dagen tot meer dan 30 dagen werd toegediend in doses die 2,5 maal de maximale dosis voor de mens bedragen. Deze effecten zouden te wijten kunnen zijn aan maternale toxiciteit (verminderde voedselconsumptie met verhoogde mortaliteit) na langdurige toediening van het geneesmiddel.
Er zijn geen aanwijzingen voor teratogene effecten waargenomen na toediening van Alfenta bij ratten of konijnen.
Er zijn geen adequate en goed gecontroleerde studies bij zwangere vrouwen. Alfenta mag alleen tijdens de zwangerschap worden gebruikt als het potentiële voordeel opweegt tegen het potentiële risico voor de foetus.
Labor and Delivery
Er zijn onvoldoende gegevens om het gebruik van Alfenta bij arbeid en bevalling te ondersteunen. Er is overdracht van het geneesmiddel via de placenta gemeld; daarom wordt gebruik bij arbeid en bevalling niet aanbevolen.
Verloskundige moeders
In één onderzoek met negen vrouwen die een postpartum tubal ligatie ondergingen, werden significante niveaus van Alfenta gedetecteerd in colostrum vier uur na toediening van 60 mcg/kg Alfenta, waarbij na 28 uur geen detecteerbare niveaus meer aanwezig waren. Voorzichtigheid is geboden wanneer Alfenta wordt toegediend aan een zogende vrouw.
Pediatrisch gebruik
Er zijn momenteel onvoldoende gegevens beschikbaar om het gebruik van Alfenta bij kinderen jonger dan 12 jaar te ondersteunen.
Bijwerkingen
De meest voorkomende bijwerkingen van opioïden zijn ademhalingsdepressie en stijfheid van de skeletspieren, met name van de rompspieren. Alfenta kan spierstijfheid veroorzaken waarbij de skeletspieren van de hals en de ledematen betrokken zijn. Zie de CLINICAL PHARMACOLOGY, WAARSCHUWINGEN en VOORZORGSMAATREGELEN voor de behandeling van ademhalingsdepressie en skeletspierrigiditeit.
Het profiel van de bijwerkingen bij 696 patiënten die Alfenta kregen voor bewaakte anesthesiezorg (MAC) is vergelijkbaar met het profiel dat is vastgesteld met Alfenta tijdens algehele anesthesie. Ademhalingsgebeurtenissen gemeld tijdens MAC omvatten hypoxie, apneu en bradypneu. Andere bijwerkingen die werden gemeld door patiënten die Alfenta kregen voor MAC, in volgorde van afnemende frequentie, waren misselijkheid, hypotensie, braken, pruritus, verwardheid, slaperigheid en agitatie.
De volgende informatie over bijwerkingen is afkomstig van gecontroleerde en open klinische onderzoeken bij 785 patiënten die intraveneuze Alfenta kregen tijdens inductie en onderhoud van algehele anesthesie. De gecontroleerde onderzoeken omvatten behandelingsvergelijkingen met fentanyl, thiopentalnatrium, enfluraan, placebo zoutoplossing en halothaan. De incidentie van bepaalde bijwerkingen wordt beïnvloed door het type gebruik, bijv. borstwandstijfheid heeft een hogere gemelde incidentie in klinische onderzoeken naar Alfentanil-inductie, en door het type operatie, bijv. misselijkheid en braken hebben een hogere gemelde incidentie bij patiënten die gynaecologische chirurgie ondergaan. De algemene meldingen van misselijkheid en braken met Alfenta waren vergelijkbaar met fentanyl.
Incidentie groter dan 1% – Waarschijnlijk oorzakelijk verband (Afgeleid van klinische onderzoeken)
| *incidentie 3% tot 9% Alle andere 1% tot 3% |
|
| Gastro-intestinaal: | misselijkheid (28%), overgeven (18%) |
| Cardiovasculair: | aritmie, bradycardie (14%), hypertensie (18%), hypotensie (10%), tachycardie (12%) |
| Musculoskeletaal: | stijfheid van de borstwand (17%), skeletspierbewegingen* |
| Respiratoir: | apneu*, postoperatieve ademhalingsdepressie |
| Centraal Zenuwstelsel: | wazig zicht, duizeligheid*, slaperigheid/ postoperatieve sedatie |
Incidentie Minder dan 1% – Waarschijnlijk Oorzakelijk verband (Afgeleid van klinische proeven)
Geweldige voorvallen gemeld bij post-marketing surveillance, niet waargenomen in klinische proeven, zijn cursief gedrukt.
| *incidentie 0.3% tot 1% | |
| Lichaam als geheel: | anafylaxie |
| Centraal Zenuwstelsel: | hoofdpijn*, myoclonische bewegingen, postoperatieve verwarring*, postoperatieve euforie*, rillingen* |
| Dermatologisch: | jeuk*, urticaria* |
| Injectieplaats: | pijn* |
| Musculoskeletaal: | skeletspierstijfheid van nek en extremiteiten |
| Respiratoir: | bronchospasme, hypercarbia*, laryngospasme* |
Drugsgebruik en -afhankelijkheid
Alfenta (Alfentanilhydrochloride) is een op lijst II geplaatste gereguleerde drug die afhankelijkheid van morfine kan veroorzaken en daarom misbruikt kan worden.
Opioïde analgetica zijn in verband gebracht met misbruik en afhankelijkheid bij zorgverleners en anderen die gemakkelijk toegang hebben tot dergelijke geneesmiddelen. Alfenta dient dienovereenkomstig te worden behandeld.
Overdosering
Overdosering zou zich manifesteren door uitbreiding van de farmacologische werking van Alfenta (Alfentanilhydrochloride) (zie KLINISCHE FARMACOLOGIE) zoals bij andere krachtige opioïde analgetica. Er is geen ervaring met overdosering met Alfenta gemeld tijdens klinische studies. De intraveneuze LD50 van Alfenta is 43-51 mg/kg bij ratten, 72-74 mg/kg bij muizen, 72-82 mg/kg bij cavia’s en 60-88 mg/kg bij honden. Intraveneuze toediening van een opioïde antagonist zoals naloxon dient te worden gebruikt als een specifiek antidotum om de ademhalingsdepressie te beheersen.
De duur van de ademhalingsdepressie na overdosering met Alfenta kan langer zijn dan de werkingsduur van de opioïde antagonist. De toediening van een opioïde antagonist mag de onmiddellijke totstandbrenging van een open luchtweg, de toediening van zuurstof en geassisteerde of gecontroleerde beademing zoals aangegeven voor hypoventilatie of apneu niet uitsluiten. Als ademhalingsdepressie gepaard gaat met spierstijfheid, kan een neuromusculair blokkerend middel nodig zijn om geassisteerde of gecontroleerde beademing mogelijk te maken. Intraveneuze vloeistoffen en vasoactieve middelen kunnen nodig zijn om hemodynamische instabiliteit te beheersen.
Alfenta dosering en toediening
De dosering van Alfenta (Alfentanilhydrochloride) moet worden geïndividualiseerd en getitreerd tot het gewenste effect bij elke patiënt op basis van het lichaamsgewicht, de lichamelijke toestand, de onderliggende pathologische aandoening, het gebruik van andere geneesmiddelen, en het type en de duur van de chirurgische ingreep en de anesthesie. Bij obese patiënten (meer dan 20% boven het ideale totale lichaamsgewicht) moet de dosering van Alfenta worden bepaald op basis van het magere lichaamsgewicht. De dosering van Alfenta dient te worden verlaagd bij oudere of verzwakte patiënten (zie VOORZORGSMAATREGELEN).
De vitale functies dienen routinematig te worden gecontroleerd.
Zie de doseringsrichtlijnen voor het gebruik van Alfenta: 1) door incrementele injectie als analgetische aanvulling op anesthesie met barbituraat/nitrous oxide/zuurstof voor korte chirurgische ingrepen (verwachte duur van minder dan een uur); 2) door continue infusie als onderhoudsanalgeticum met nitrous oxide/zuurstof voor algemene chirurgische ingrepen; en 3) door intraveneuze injectie in anesthesiedoses voor de inductie van anesthesie voor algemene chirurgische ingrepen met een verwachte duur van ten minste 45 minuten; en 4) door intraveneuze injectie als analgetisch bestanddeel voor bewaakte anesthesiezorg (MAC).
| DOSERING MOET WORDEN GEÏNDIVIDUALISEERD EN GETITREERD | |
|---|---|
| VOOR GEBRUIK DURING VAN ALGEMENE ANESTHESIE | |
| SPONTANEEL BEademING/ASSISTIEVE VENTILATIE | Inductie van Analgesie: 8-20 mcg/kg Onderhoud van Analgesie: 3-5 mcg/kg q 5-20 min of 0.5 tot 1 mcg/kg/min Totale dosis: 8-40 mcg/kg |
| ASSISTED OR CONTROLLED VENTILATION | |
| Incrementele Injectie (Om de reactie op laryngoscopie en intubatie te verzwakken) |
Inductie van Analgesie: 20-50 mcg/kg Onthouden van analgesie: 5-15 mcg/kg q 5-20 min Totale dosis: Tot 75 mcg/kg |
| Continue infusie (Om de reactie op intubatie en incisie te dempen) |
Infusiesnelheden zijn variabel en moeten worden getitreerd op het gewenste klinische effect. Zie de infuusrichtlijnen hieronder. Inductie van analgesie: 50-75 mcg/kg Behoud van analgesie: 0,5 tot 3 mcg/kg/min (Gemiddelde dosis 1 tot 1,5 mcg/kg/min) Totale dosis: Afhankelijk van de duur van de procedure |
| Anesthetische Inductie | Inductie van Anesthesie: 130-245 mcg/kg Onderhoud van Anesthesie: 0,5 tot 1,5 mcg/kg/min of algehele anesthesie Totale dosis: Afhankelijk van de duur van de procedure Bij deze doses moet truncale rigiditeit worden verwacht en moet een spierverslapper worden gebruikt. Toedienen langzaam (gedurende 3 minuten). Concentratie van inhalatiemiddelen verlaagd met 30-50% gedurende het eerste uur. |
| GEMIDDELDE ANESTHESIEVERZORGING (MAC) (Voor gesedeerde en responsieve, spontaan ademende patiënten) |
Inductie van MAC: 3-8 mcg/kg Houding van MAC: 3-5 mcg/kg q 5-20 min of 0.25 tot 1 mcg/kg/min Totale dosis: 3-40 mcg/kg |
Continue infusie: 0,5-3 mcg/kg/min toegediend met lachgas/zuurstof bij patiënten die een algemene operatie ondergaan. Na een anesthesie-inductiedosis Alfenta worden de infusiesnelheden gedurende het eerste onderhoudsuur met 30-50% verlaagd.
Verschommelingen in de vitale functies die wijzen op een reactie op chirurgische stress of op verlichting van de anesthesie kunnen onder controle worden gehouden door de hoeveelheid Alfentanil te verhogen tot maximaal 4 mcg/kg/min en/of door bolusdoses van 7 mcg/kg toe te dienen. Als veranderingen niet onder controle zijn na drie bolusdoses gegeven over een periode van vijf minuten, dient een barbituraat, vasodilatator en/of inhalatiemiddel te worden gebruikt. De infusiesnelheid moet altijd naar beneden worden bijgesteld als deze verschijnselen zich niet voordoen, totdat er enige respons is op chirurgische stimulatie.
In plaats van de infusiesnelheid te verhogen, moeten bolusdoses Alfenta van 7 mcg/kg of een krachtig inhalatiemiddel worden toegediend als reactie op verschijnselen van verlichting van de anesthesie tijdens de laatste 15 minuten van de operatie. De Alfenta-infusie dient ten minste 10-15 minuten voor het einde van de operatie te worden gestaakt.
Gebruik bij kinderen
Clinische gegevens ter ondersteuning van het gebruik van Alfenta bij patiënten jonger dan 12 jaar zijn op dit moment niet beschikbaar. Daarom wordt dergelijk gebruik niet aanbevolen.
Premedicatie
De selectie van preanesthetische medicatie dient te worden gebaseerd op de behoeften van de individuele patiënt.
Neuromusculaire blokkeringsmiddelen
De geselecteerde neuromusculaire blokkeringsmiddelen dienen compatibel te zijn met de toestand van de patiënt, rekening houdend met de hemodynamische effecten van een bepaalde spierverslapper en de vereiste mate van ontspanning van de skeletspieren (zie de rubrieken KLINISCHE FARMACOLOGIE, WAARSCHUWINGEN en VOORZORGSMAATREGELEN).
Bij patiënten die anesthesiedoseringen (inductie) van Alfenta toegediend krijgen, is het van essentieel belang dat gekwalificeerd personeel en adequate faciliteiten beschikbaar zijn voor de behandeling van intraoperatieve en postoperatieve ademhalingsdepressie.
Zie ook de rubrieken WAARSCHUWINGEN en VOORZORGSMAATREGELEN.
Voor het nauwkeurig toedienen van kleine volumes Alfenta wordt het gebruik van een tuberculinespuit of equivalent aanbevolen.
De fysische en chemische compatibiliteit van Alfenta is aangetoond in oplossing met normale zoutoplossing, 5% dextrose in normale zoutoplossing, 5% dextrose in water en Lactated Ringers. Klinische studies van Alfenta infusie zijn uitgevoerd met Alfenta verdund tot een concentratiebereik van 25 mcg/mL tot 80 mcg/mL.
Als voorbeeld van de bereiding van Alfenta voor infusie, 20 mL Alfenta toegevoegd aan 230 mL verdunningsmiddel levert 40 mcg/mL oplossing van Alfenta op.
Parenterale geneesmiddelen dienen vóór toediening visueel te worden geïnspecteerd op deeltjes en verkleuring, wanneer de oplossing en de verpakking dit toelaten.
Veiligheid EN BEHANDELING
Alfenta (Alfentanilhydrochloride) wordt geleverd in individueel verzegelde toedieningsvormen die geen bekend risico vormen voor zorgverleners die incidenteel contact hebben. Accidentele blootstelling van de huid aan Alfenta dient te worden behandeld door het getroffen gebied met water af te spoelen.
Beschermen tegen licht. Bewaren: Bewaren bij 20° tot 25°C (68° tot 77°F). .
Hoe wordt Alfenta geleverd
Alfenta (Alfentanilhydrochloride) Injectie voor intraveneus gebruik. Elke ml bevat: Actief: Alfentanil basis 500 mcg. Inactieven: Natriumchloride 9 mg en WFI Q.S Alfenta Injectie is verkrijgbaar als:
NDC 11098-060-02, 2 ml Ampul in verpakkingen van 10
NDC 11098-060-05, 5 ml Ampul in verpakkingen van 10
NDC 11098-060-10, 10 ml Ampul in verpakkingen van 5
NDC 11098-060-20, 20 ml Ampul in verpakkingen van 5
U.S. Patent No. 4,167,574
Mei 1995, November 1995
TAYLOR PHARMACEUTICALS
AN AKORN COMPANY
Decatur, IL 62522
AFA0N Rev. 06/05
| Alfenta Alfentanilhydrochloride injectie |
|||||||||||||||||||||||||||||||
|
|||||||||||||||||||||||||||||||
|
|||||||||||||||||||||||||||||||
|
|||||||||||||||||||||||||||||||
|
|||||||||||||||||||||||||||||||
Etiketteerder – TAYLOR PHARMACEUTICALS