Aplastic anemia pathophysiology
Aplastic anemia Microchapters
Home
Patient Information
Overview
Historical Perspective
Classification
Pathophysiology
Causes
Differentiating Aplastische anemie van other Diseases
Epidemiology and Demographics
Risk Factors
Screening
Natural History, Complications and Prognosis
Diagnosis
Diagnostic Study of Choice
History and Symptoms
Physical Examination
Laboratory Findings
Electrocardiogram
Chest X Ray
CT
MRI
Echocardiography or Ultrasound
Other Imaging Findings
Other Diagnostic Studies
Treatment
Medical Therapy
Surgery
Primary Prevention
Secondary Prevention
Cost-Effectiveness of Therapy
Future or Investigational Therapies
Case Studies
Case #1
Aplastic anemia pathophysiology On the Web
Most recent articles
cited articles
Review articles
CME Programs
Powerpoint dia’s
afbeeldingen
American Roentgen Ray Society Afbeeldingen van Aplastische anemie pathofysiologie
Alle afbeeldingen X-röntgenstralen Echo & Echografie CT-beelden MRI
Ongaande trials bij Clinical Trials.gov
US National Guidelines Clearinghouse
NICE Guidance
FDA over de pathofysiologie van aplastische anemie
CDC over de pathofysiologie van aplastische anemie
Aplastische anemie pathofysiologie in het nieuws
Blogs over Aplastische anemie pathofysiologie
Directies naar ziekenhuizen Behandeling van aplastische anemie
Risicocalculatoren en risicofactoren voor Aplastische anemie pathofysiologie
Editor-Hoofdredacteur: C. Michael Gibson, M.S., M.D. ; Medewerkend hoofdredacteur(s)/hoofdredacteur: Priyamvada Singh, M.D. Nazia Fuad M.D.
Help WikiDoc door hier inhoud toe te voegen. Het is gemakkelijk! Klik hier om meer te leren over bewerken.
Overzicht
Het beenmerg is een sponsachtig weefsel, dat zich in de sponsachtige of spongieuze delen van botten bevindt. Het is sterk gevasculariseerd en rijk geïnnerveerd Beenmerg is de voornaamste plaats van hematopoëse en bestaat uit hematopoiëtische cellen, beenmergvetweefsel en stromale cellen. Het meest bepalende kenmerk in de pathofysiologie van aplastische anemie is het verlies van hematopoietische stamcellen. Dit kan de vorm aannemen van hematopoietisch falen of van immuungemedieerde vernietiging van het beenmerg. Geneesmiddelen, chemicaliën, virussen en verschillende soorten mutaties veranderen het immunologische uiterlijk van HSC’s, wat leidt tot auto-immune vernietiging van beenmergcellen. AA kan zich geleidelijk ontwikkelen tot andere hematologische aandoeningen, waaronder paroxismale nachtelijke hemoglobinurie, myelodysplastische syndromen en acute myeloïde leukemie.) Klonale evolutie bij AA kan optreden ten gevolge van mutaties of cytogenetische afwijkingen. De genen die vaak gemuteerd blijken te zijn, zijn DMNT3A, ASXL1, BCOR, BCORL1, PIGA.
Pathofysiologie
Physiologie
De normale fysiologie van het beenmerg kan als volgt worden begrepen:
- Het beenmerg is een sponsachtig weefsel, dat zich in de sponsachtige of spongieuze delen van beenderen bevindt
- Het is sterk gevasculariseerd en rijk geïnnerveerd
- Het beenmerg is de primaire plaats van hematopoëse.
- Het is samengesteld uit hematopoietische cellen, merg vetweefsel, en stromale cellen.
- Hematopoietische stamcellen (HSC) in het beenmerg zijn de bron van alle rijpe cellen in het perifere bloed en de weefsels en zijn multipotent.
- HSC worden herkend en geïsoleerd op basis van hun immunofenotype.
- HSC’s vormen een kleine populatie binnen de CD34+/CD38-fractie van beenmergcellen.
- De hematopoiese wordt gecontroleerd door verschillende regulerende mechanismen, waaronder groeifactoren.
- De normale beenmergstructuur kan worden beschadigd of verplaatst door aplastische anemie, maligniteiten of infecties.
- Dit leidt tot een verminderde productie van bloedcellen en bloedplaatjes.
Pathogenese
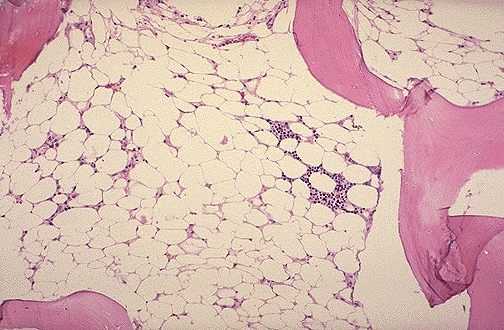
Het meest defenitieve kenmerk in de pathofysiologie van aplastische anemie is het verlies van hematopoietische stamcellen.
Pathofysiologische mechanismen die resulteren in verlies van HSC’s en aplastische anemie veroorzaken, zijn onder meer:
Hematopoietisch falen
- CD34-cellen zijn bijna afwezig bij aplastische anemie.
- Progenitorcellen die in staat zijn erytroïde, myeloïde en megakaryocytaire cellen te vormen, zijn sterk verminderd.
- De primitieve hematopoietische cellen die nauw verwant zijn aan stamcellen zijn consistent deficiënt.
- De witte bloedcellen in aplastische anemie hebben korte telomeren.
- Telomeren zijn herhalingen aan het einde van eukaryotische chromosomen en zijn essentieel voor chromosoom bescherming en volledige DNA replicatie.
Immuungemedieerde T-celvernietiging van het beenmerg
-
- Geneesmiddelen, chemicaliën, virussen en verschillende soorten mutaties veranderen het immunologische uiterlijk van HSC’s, wat leidt tot auto-immuunvernietiging van beenmergcellen.
- Bij patiënten met verworven aplastische anemie zijn lymfocyten verantwoordelijk voor de vernietiging van de hematopoietische cellen.
- Deze T-cellen produceren een remmende factor, interferonen , tumor necrose factor, en interleukine-2, resulterend in hematopoietische celdood door apoptose.
- CD4+CD25+FOXP3+ regulatoire T-cellen zijn deficiënt bij deze patiënten, vergelijkbaar met wat gezien wordt bij andere auto-immuunziekten.
- Deficiëntie van deze regulatoire T-cellen resulteert in toename van T-bet eiwitniveaus in T-cellen, toename van interferon (IFN)-γ,2 en stamcelvernietiging.
- Een verhoogde immuunrespons, waaronder tumornecrosefactor -α, IFNγ, en interleukine-6, komt ook veel voor bij AA-patiënten.
Clonale evolutie
- AA kan zich geleidelijk ontwikkelen tot andere hematologische aandoeningen, waaronder
-
- Paroxysmale nachtelijke hemoglobinurie
- Myelodysplastische syndromen
- Acute myeloïde leukemie
- Clonale evolutie bij AA kan optreden als gevolg van mutaties of cytogenetische afwijkingen.
- De genen die vaak gemuteerd blijken te zijn, zijn
- DMNT3A
- ASXL1
- BCOR
- BCORL1
- PIGA
Genetica
Genen die betrokken zijn bij de pathogenese van aplastische anemie zijn onder andere:
- HLA-DR15
- CD4+ CD25+ FOXP3+ regulatoire T-cellen
- STAT3
- TERT
- TERC
Geassocieerde aandoeningen
Aplastische anemie is geassocieerd met de volgende aandoeningen:
- Anemie van Franconi
- PNH Paroxysmale Nachtelijke Hemoglobinurie
Grote Pathologie
Aplastische anemie vertoont vertoont geen bruto pathologie
Microscopische Pathologie
In aplastische anemie vertoont beenmergmicroscopie hypo en zelfs acellulariteit, vetweefsel en bleek stroma.
- Hays K (februari 1990). “Fysiologie van normaal beenmerg”. Semin Oncol Nurs. 6 (1): 3-8. PMID 2406826.
- Bacigalupo A (2007). “Aplastische anemie: pathogenese en behandeling”. Hematology Am Soc Hematol Educ Program: 23–8. doi:10.1182/asheducation-2007.1.23. PMID 18024605.
- 3.0 3.1 3.2 3.3 Brodsky, R. A. (2000). “Aplastische Anemie: Pathophysiology and Treatment”. Journal of the National Cancer Institute. 92 (9): 754-754. doi:10.1093/jnci/92.9.754. ISSN 1460-2105.
- 4.0 4.1 Young, Neal S. (2002). “Acquired Aplastic Anemia”. Annals of Internal Medicine. 136 (7): 534. doi:10.7326/0003-4819-136-7-200204020-00011. ISSN 0003-4819.