Alfenta
Nazwa ogólna: Alfentanil hydrochloride
Postać dawkowania: iniekcja
Medically reviewed by Drugs.com. Ostatnia aktualizacja 22 stycznia 2021.
- Skutki uboczne
- Dawkowanie
- Profesjonaliści
- Interakcje
- Ciąża
- Więcej
.
CII
Rx only
- Alfenta Opis
- Alfenta – Farmakologia kliniczna
- Wskazania i stosowanie produktu Alfenta
- Przeciwwskazania
- Ostrzeżenia
- Środki ostrożności
- Ogólne
- Urazy głowy
- Zaburzone oddychanie
- Niedobra czynność wątroby lub nerek
- Interakcje lekowe
- Karcynogeneza, mutageneza i upośledzenie płodności
- Kategoria ciążowa C
- Praca i poród
- Karmiące matki
- Stosowanie u dzieci
- Działania niepożądane
- Występowanie większe niż 1% – prawdopodobnie związane z przyczyną (pochodzące z badań klinicznych)
- Występowanie Mniej niż 1% – Prawdopodobnie związane przyczynowo (Uzyskane z badań klinicznych)
- Nadużywanie i uzależnienie od leków
- Przedawkowanie
- Alfenta dawkowanie i podawanie
- Stosowanie u dzieci
- Premedykacja
- Środki blokujące przewodnictwo nerwowo-mięśniowe
- BEZPIECZEŃSTWO I POSTĘPOWANIE
- How is Alfenta Supplied
Alfenta Opis
Alfenta (Alfentanil hydrochloride) Injection jest opioidowym lekiem przeciwbólowym oznaczonym chemicznie jako N-.-4-(metoksymetylo)-4-piperydynylo]-N-fenylopropanamidu monohydrochlorku (1:1) o masie cząsteczkowej 452.98 i współczynniku podziału n-oktanol:woda wynoszącym 128:1 przy pH 7,4. Wzór strukturalny Alfenty to:
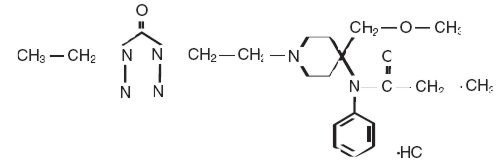
Alfenta jest sterylnym, niepirogennym, wolnym od środków konserwujących roztworem wodnym zawierającym Alfentanilu chlorowodorek równoważny 500 µg na mL bazy Alfentanilu do wstrzykiwań dożylnych. Roztwór, który zawiera chlorek sodu dla zachowania izotoniczności, ma pH w zakresie 4-6. Każdy mL zawiera: Substancję czynną: Alfentanil base 500 mcg. Nieaktywne: Sodium Chloride 9 mg and Water for Injection Q.S.
Alfenta – Farmakologia kliniczna
Alfenta (Alfentanilu chlorowodorek) jest opioidowym lekiem przeciwbólowym o szybkim początku działania.
W przypadku dłuższych zabiegów dawki do 75 mcg/kg osłabiają hemodynamiczne reakcje na laryngoskopię, intubację i nacięcie, z czasem powrotu do zdrowia porównywalnym z fentanylem. W dawkach 50-75 mcg/kg, po których następuje ciągły wlew 0,5-3 mcg/kg/min, Alfenta łagodzi odpowiedź katecholaminową z szybszym powrotem do zdrowia i zmniejszonym zapotrzebowaniem na pooperacyjne leki przeciwbólowe w porównaniu z pacjentami, którym podawano enfluran. W dawkach 5 mcg/kg Alfenta zapewnia analgezję u przytomnego, ale uspokojonego pacjenta. W zależności od reakcji pacjenta, może być konieczne zastosowanie dawek większych niż 5 mcg/kg. Pacjenci w podeszłym wieku lub osłabieni mogą wymagać mniejszych dawek. Zgłaszano dużą zmienność wewnątrz- i międzyprzedmiotową w farmakokinetycznym rozkładzie produktu Alfenta.
Farmakokinetykę produktu Alfenta można opisać jako model trójkompartmentowy z okresami półtrwania dystrybucji sekwencyjnej wynoszącymi 1 i 14 minut; oraz końcowym okresem półtrwania eliminacji wynoszącym 90-111 minut (w porównaniu z końcowym okresem półtrwania eliminacji wynoszącym około 475 minut dla fentanylu i około 265 minut dla sufentanilu w dawkach 250 mcg). Wątroba jest głównym miejscem biotransformacji.
Alfenta ma pozorną objętość dystrybucji wynoszącą 0,4-1 L/kg, co stanowi około jedną czwartą do jednej dziesiątej objętości dystrybucji fentanylu, ze średnim klirensem osoczowym wynoszącym 5 mL/kg/min w porównaniu z około 8 mL/kg/min dla fentanylu.
Tylko 1,0% dawki jest wydalane w postaci niezmienionego leku; wydalanie z moczem jest główną drogą eliminacji metabolitów. Wiązanie Alfenty z białkami osocza wynosi około 92%.
W jednym badaniu z udziałem 15 pacjentów, którym podawano Alfentę z podtlenkiem azotu/tlenem, wykazano, że wąski zakres stężeń Alfenty w osoczu, około 310-340 ng/ml, zapewnia odpowiednie znieczulenie do operacji wewnątrzbrzusznych, podczas gdy niższe stężenia, około 190 ng/ml, blokowały reakcje na zamknięcie skóry. Stężenia w osoczu pomiędzy 100-200 ng/mL zapewniały odpowiednie znieczulenie w przypadku powierzchownych zabiegów chirurgicznych.
Alfenta ma natychmiastowy początek działania. W dawkach około 105 mcg/kg, Alfenta wytwarza hipnozę, jak określono przez wzorce EEG; anestetyczne ED90 z 182 mcg/kg dla Alfenta w nieleczonych pacjentów została określona, w oparciu o zdolność do blokowania odpowiedzi na umieszczenie nosogardła dróg oddechowych. Na podstawie badań klinicznych, wymagania dotyczące dawki indukcyjnej wynoszą od 130-245 mcg/kg. W przypadku zabiegów trwających 30-60 minut, dawki nasycające do 50 mcg/kg powodują reakcję hemodynamiczną na intubację dotchawiczą i nacięcie skóry porównywalną do reakcji na fentanyl. Przedintubacyjna dawka nasycająca 50-75 mcg/kg przed wlewem ciągłym łagodzi reakcję na laryngoskopię, intubację i nacięcie. Późniejsze podanie wlewu Alfenta podawanego z szybkością 0,5-3 mcg/kg/min z podtlenkiem azotu/tlenem łagodzi reakcje współczulne na stres chirurgiczny z szybszym powrotem do zdrowia niż enfluran.
Zapotrzebowanie na lotne wziewne środki znieczulające zostało zmniejszone o trzydzieści do pięćdziesięciu procent podczas pierwszych 60 minut podtrzymywania u pacjentów, którym podano dawki znieczulające (powyżej 130 mcg/kg) Alfenty w porównaniu z pacjentami, którym podano dawki 4-5 mg/kg tiopentalu do indukcji znieczulenia. W dawkach indukujących znieczulenie, Alfenta zapewnia głęboki poziom znieczulenia podczas pierwszej godziny podtrzymywania znieczulenia i zapewnia osłabienie odpowiedzi hemodynamicznej podczas intubacji i nacinania.
Po podaniu dawki indukującej znieczulenie Alfenta, wymagania dotyczące infuzji Alfenty są zmniejszone o 30 do 50% przez pierwszą godzinę podtrzymywania.
Stwierdzono, że u pacjentów z upośledzoną czynnością wątroby oraz u pacjentów w wieku powyżej 65 lat występuje zmniejszony klirens osoczowy i wydłużony okres końcowej eliminacji produktu Alfenta, co może wydłużać okres rekonwalescencji pooperacyjnej. Powtarzane lub ciągłe podawanie produktu Alfenta powoduje zwiększenie stężenia leku w osoczu i jego kumulację, szczególnie u pacjentów ze zmniejszonym klirensem osoczowym.
Bradykardia może być obserwowana u pacjentów, którym podawano produkt Alfenta. Częstość występowania i stopień bradykardii mogą być bardziej wyraźne, gdy Alfenta jest podawana w skojarzeniu z niewagolitycznymi środkami blokującymi przewodnictwo nerwowo-mięśniowe lub w przypadku braku środków antycholinergicznych, takich jak atropina.
Podanie dożylne diazepamu bezpośrednio przed lub po podaniu dużych dawek produktu Alfenta spowodowało obniżenie ciśnienia krwi, które może być wtórne do rozszerzenia naczyń; powrót do zdrowia może być również wydłużony.
Pacjenci, którym podawano dawki do 200 mcg/kg produktu Alfenta, nie wykazywali znaczącego zwiększenia stężenia histaminy ani klinicznych dowodów uwalniania histaminy.
Sztywność mięśni szkieletowych jest związana z dawką i szybkością podawania produktu Alfenta. Sztywność mięśni wystąpi z natychmiastowym początkiem po podaniu dawek indukujących znieczulenie. Środki zapobiegawcze (patrz OSTRZEŻENIA) mogą zmniejszyć szybkość i nasilenie.
Czas trwania i stopień depresji oddechowej oraz zwiększony opór dróg oddechowych zwykle zwiększają się wraz z dawką, ale obserwowano je również przy mniejszych dawkach. Chociaż większe dawki mogą powodować bezdech i dłuższy czas trwania depresji oddechowej, bezdech może również wystąpić przy małych dawkach.
Podczas monitorowanej opieki anestezjologicznej (MAC) należy zwrócić uwagę na działanie Alfenta Injection na układ oddechowy. Może wystąpić zmniejszenie wysycenia tlenem, bezdech, zmniejszenie częstości oddechów i niedrożność górnych dróg oddechowych. (Patrz OSTRZEŻENIA)
Wskazania i stosowanie produktu Alfenta
Alfenta (Alfentanilu chlorowodorek) jest wskazana:
jako środek przeciwbólowy podawany w dawkach przyrostowych w podtrzymywaniu znieczulenia za pomocą barbituranu/podtlenku azotu/tlenu. jako środek przeciwbólowy podawany w ciągłej infuzji z podtlenkiem azotu/tlenem w podtrzymywaniu znieczulenia ogólnego. jako podstawowy środek anestetyczny do indukcji znieczulenia u pacjentów poddawanych zabiegom chirurgii ogólnej, u których wymagana jest intubacja dotchawicza i wentylacja mechaniczna. jako składnik analgetyczny w monitorowanej opiece anestezjologicznej (MAC).
SEE DOSAGE CHART FOR MORE COMPLETE INFORMATION ON THE USE OF Alfenta.
Przeciwwskazania
Alfenta (Alfentanilu chlorowodorek) jest przeciwwskazana u pacjentów ze znaną nadwrażliwością na lek lub znaną nietolerancją na innych agonistów opioidowych.
Ostrzeżenia
Alfenta POWINNA BYĆ PODAWANA TYLKO PRZEZ OSOBY SPECJALNIE PRZESZKOLONE W STOSOWANIU ŚRODKÓW ANESTEZJOLOGICZNYCH I OGÓLNYCH ORAZ W ZARZĄDZANIU EFEKTAMI ODDECHOWYMI SILNYCH OPIOIDÓW.
ANTAGONISTA OPIOIDÓW, SPRZĘT DO RESUSCYTACJI I INTUBACJI ORAZ TLEN POWINNY BYĆ ŁATWO DOSTĘPNE.
ZE WZGLĘDU NA MOŻLIWOŚĆ WYSTĄPIENIA OPÓŹNIONEJ DEPRESJI ODDECHOWEJ, MONITOROWANIE PACJENTA MUSI BYĆ KONTYNUOWANE PRZEZ DŁUGI CZAS PO ZABIEGU.
Alfenta (Alfentanilu chlorowodorek) podawana w dawkach początkowych do 20 mcg/kg może powodować sztywność mięśni szkieletowych, szczególnie mięśni trójgłowych. Częstość występowania i nasilenie sztywności mięśni jest zwykle związane z dawką. Podanie produktu Alfenta w dawkach indukujących znieczulenie (powyżej 130 mcg/kg) konsekwentnie powoduje sztywność mięśni o natychmiastowym początku. Początek sztywności mięśni występuje wcześniej niż w przypadku innych opioidów. Alfenta może powodować sztywność mięśni, która obejmuje wszystkie mięśnie szkieletowe, w tym mięśnie szyi i kończyn. Częstość występowania może być zmniejszona przez: 1) rutynowe metody podawania środków blokujących przewodnictwo nerwowo-mięśniowe w przypadku zrównoważonego znieczulenia opioidowego; 2) podanie do 1/4 pełnej dawki paraliżującej środka blokującego przewodnictwo nerwowo-mięśniowe tuż przed podaniem produktu Alfenta w dawkach do 130 mcg/kg; po utracie przytomności należy podać pełną dawkę paraliżującą środka blokującego przewodnictwo nerwowo-mięśniowe; lub 3) jednoczesne podawanie produktu Alfenta i pełnej dawki paraliżującej środka blokującego przewodnictwo nerwowo-mięśniowe, gdy produkt Alfenta jest stosowany w szybko podawanych dawkach znieczulających (powyżej 130 mcg/kg).
Używany środek blokujący przewodnictwo nerwowo-mięśniowe powinien być odpowiedni do stanu układu krążenia pacjenta. Powinny być dostępne odpowiednie urządzenia do pooperacyjnego monitorowania i wentylacji pacjentów, którym podano Alfentę. Istotne jest, aby urządzenia te były w pełni wyposażone do obsługi wszystkich stopni depresji oddechowej.
PACJENCI OTRZYMUJĄCY MONITOROWANĄ OPIEKĘ ANESTEZJOLOGICZNĄ (MAC) POWINNI BYĆ STALE MONITOROWANI PRZEZ OSOBY NIEZAANGAŻOWANE W PRZEPROWADZANIE PROCEDURY CHIRURGICZNEJ LUB DIAGNOSTYCZNEJ; SUPLEMENTACJA TLENU POWINNA BYĆ NATYCHMIAST DOSTĘPNA I PODAWANA, GDY JEST TO WSKAZANE KLINICZNIE; SATURACJA TLENEM POWINNA BYĆ STALE MONITOROWANA; PACJENT POWINIEN BYĆ OBSERWOWANY POD KĄTEM WCZESNYCH OBJAWÓW NIEDOCIŚNIENIA, BEZDECHU, NIEDROŻNOŚCI GÓRNYCH DRÓG ODDECHOWYCH I (LUB) DESATURACJI TLENU.
Szerokie i nieprzewidywalne nasilenie działania inhibitorów monoaminooksydazy (MAO) zgłaszano w przypadku innych opioidowych leków przeciwbólowych, rzadko w przypadku alfentanilu. Dlatego też w przypadku podawania alfentanilu pacjentom, którzy w ciągu 14 dni otrzymywali inhibitory MAO, zaleca się odpowiednie monitorowanie i gotowość do podania leków rozszerzających naczynia krwionośne i beta-adrenolityków w leczeniu nadciśnienia tętniczego.
Środki ostrożności
Zgłaszano również opóźnioną depresję oddechową, zaostrzenie zapalenia dróg oddechowych, BRADYKARDIĘ, ASYSTOLIĘ, ARYTMIĘ I NADCIŚNIENIE. Dlatego należy stale monitorować objawy życiowe.
Ogólne
Dawkę początkową produktu Alfenta (Alfentanilu chlorowodorek) należy odpowiednio zmniejszyć u pacjentów w podeszłym wieku i osłabionych. Przy ustalaniu dawek uzupełniających należy uwzględnić wpływ dawki początkowej. U pacjentów otyłych (ponad 20% powyżej idealnej całkowitej masy ciała), dawkę produktu Alfenta należy ustalić na podstawie beztłuszczowej masy ciała.
W jednym badaniu klinicznym dawka produktu Alfenta wymagana do wywołania znieczulenia, określona przez pojawienie się fal delta w EEG, była o 40% mniejsza u pacjentów geriatrycznych niż dawka potrzebna u zdrowych młodych pacjentów.
U pacjentów z upośledzoną czynnością wątroby oraz u pacjentów geriatrycznych klirens osoczowy produktu Alfenta może być zmniejszony, a powrót do zdrowia po zabiegu może być wydłużony.
Dawki indukcyjne produktu Alfenta należy podawać powoli (w ciągu trzech minut). Podanie może spowodować utratę napięcia naczyniowego i niedociśnienie. Należy rozważyć wymianę płynów przed indukcją.
Diazepam podawany bezpośrednio przed lub w połączeniu z dużymi dawkami produktu Alfenta może powodować rozszerzenie naczyń, niedociśnienie i skutkować opóźnionym powrotem do zdrowia.
Bradykardię wywołaną produktem Alfenta można leczyć atropiną. Ciężka bradykardia i asystolia były z powodzeniem leczone atropiną i konwencjonalnymi metodami resuscytacyjnymi.
Wybór środka do blokady nerwowo-mięśniowej powinien uwzględniać hemodynamiczne działanie danego środka zwiotczającego mięśnie oraz wymagany stopień zwiotczenia mięśni szkieletowych.
Po podaniu indukcyjnej dawki znieczulenia produktem Alfenta, zapotrzebowanie na lotne anestetyki wziewne lub infuzję produktu Alfenta zmniejsza się o 30 do 50% przez pierwszą godzinę podtrzymywania.
Infuzję produktu Alfenta należy przerwać co najmniej 10-15 minut przed zakończeniem zabiegu podczas znieczulenia ogólnego. Podczas podawania produktu Alfenta w ramach monitorowanej opieki anestezjologicznej (MAC), infuzje można kontynuować do końca zabiegu.
Depresja oddechowa spowodowana opioidowymi lekami przeciwbólowymi może być odwrócona przez antagonistów opioidów, takich jak nalokson. Ponieważ czas trwania depresji oddechowej wywołanej przez Alfentę może trwać dłużej niż czas działania antagonisty opioidowego, należy prowadzić odpowiedni nadzór. Podobnie jak w przypadku wszystkich silnych opioidów, głębokiej analgezji towarzyszy depresja oddechowa i zmniejszenie wrażliwości na stymulację CO2, które mogą utrzymywać się do okresu pooperacyjnego lub wystąpić ponownie w tym okresie. Śródoperacyjna hiperwentylacja może dodatkowo zmienić pooperacyjną odpowiedź na CO2. Należy zastosować odpowiednie monitorowanie pooperacyjne, szczególnie po wlewach i dużych dawkach produktu Alfenta, w celu zapewnienia, że odpowiednie oddychanie spontaniczne jest ustalone i utrzymywane przy braku stymulacji przed wypisaniem pacjenta z sali pooperacyjnej.
Urazy głowy
Alfenta powinna być stosowana z ostrożnością u pacjentów z urazem głowy lub zwiększonym ciśnieniem wewnątrzczaszkowym, ze względu na zwiększone ryzyko depresji oddechowej. Podobnie jak wszystkie opioidy, Alfenta może zaciemniać przebieg kliniczny u pacjentów z urazami głowy i powinna być stosowana tylko wtedy, gdy jest to wskazane klinicznie.
Zaburzone oddychanie
Alfenta powinna być stosowana z ostrożnością u pacjentów z chorobą płuc, zmniejszoną rezerwą oddechową lub potencjalnie upośledzonym oddychaniem. U takich pacjentów opioidy mogą dodatkowo zmniejszać napęd oddechowy i zwiększać opór dróg oddechowych. Podczas znieczulenia można sobie z tym poradzić poprzez wspomagane lub kontrolowane oddychanie.
Niedobra czynność wątroby lub nerek
U pacjentów z zaburzeniami czynności wątroby lub nerek, produkt Alfenta należy podawać ostrożnie ze względu na znaczenie tych narządów w metabolizmie i wydalaniu produktu Alfenta.
Interakcje lekowe
Zarówno wielkość, jak i czas trwania działania na ośrodkowy układ nerwowy i układ sercowo-naczyniowy mogą być zwiększone, gdy Alfenta jest podawana w skojarzeniu z innymi lekami działającymi depresyjnie na OUN, takimi jak barbiturany, leki uspokajające, opioidy lub wziewne środki znieczulenia ogólnego. Pooperacyjna depresja oddechowa może być wzmocniona lub przedłużona przez te środki. W takich przypadkach leczenia skojarzonego należy zmniejszyć dawkę jednego lub obu środków. Ograniczone doświadczenie kliniczne wskazuje, że zapotrzebowanie na lotne wziewne środki znieczulające jest zmniejszone o 30 do 50% przez pierwsze sześćdziesiąt (60) minut po indukcji produktem Alfenta.
Współczesne stosowanie erytromycyny z produktem Alfenta może znacząco hamować klirens produktu Alfenta i może zwiększać ryzyko przedłużonej lub opóźnionej depresji oddechowej.
Cymetydyna zmniejsza klirens produktu Alfenta. Dlatego przy dłuższym podawaniu wymagane będą mniejsze dawki produktu Alfenta, a czas działania produktu Alfenta może ulec wydłużeniu.
Przedoperacyjne podawanie leków wpływających na wątrobowy przepływ krwi lub czynność enzymów może zmniejszyć klirens osoczowy i wydłużyć okres rekonwalescencji.
Karcynogeneza, mutageneza i upośledzenie płodności
Nie przeprowadzono długoterminowych badań produktu Alfenta na zwierzętach w celu oceny potencjału rakotwórczego. Nie stwierdzono mutacji chromosomów strukturalnych w teście mikrojądrowym in vivo u samic szczurów przy podawaniu pojedynczych dożylnych dawek produktu Alfenta wynoszących 20 mg/kg masy ciała (około 40 razy więcej niż górna dawka u ludzi), co odpowiada dawce 103 mg/m2 powierzchni ciała. W teście dominującej letalności in vivo u samców i samic myszy przy maksymalnej dawce dożylnej wynoszącej 20 mg/kg (60 mg/m2) nie uzyskano dominujących mutacji letalnych. Nie ujawniono działania mutagennego w teście Amesa Salmonella typhimurium in vitro, z aktywacją metaboliczną i bez aktywacji metabolicznej.
Kategoria ciążowa C
Wykazano, że alfenta wywiera działanie embriobójcze u szczurów i królików, gdy jest podawana w dawkach 2,5 razy większych od górnej dawki stosowanej u ludzi przez okres od 10 dni do ponad 30 dni. Skutki te mogły być spowodowane toksycznością matczyną (zmniejszenie spożycia pokarmu ze zwiększoną śmiertelnością) po długotrwałym podawaniu leku.
Nie zaobserwowano dowodów działania teratogennego po podaniu produktu Alfenta u szczurów lub królików.
Nie ma odpowiednich i dobrze kontrolowanych badań u kobiet w ciąży. Alfenta powinna być stosowana w czasie ciąży tylko wtedy, gdy potencjalne korzyści uzasadniają potencjalne ryzyko dla płodu.
Praca i poród
Brak wystarczających danych potwierdzających stosowanie produktu Alfenta w czasie pracy i porodu. Zgłaszano przenoszenie leku przez łożysko; dlatego nie zaleca się stosowania w czasie porodu i połogu.
Karmiące matki
W jednym z badań z udziałem dziewięciu kobiet poddanych poporodowemu podwiązaniu jajowodów, znaczące poziomy Alfenty wykryto w siarze cztery godziny po podaniu 60 mcg/kg Alfenty, przy czym po 28 godzinach nie wykryto żadnych wykrywalnych poziomów. Należy zachować ostrożność w przypadku podawania produktu Alfenta kobietom karmiącym piersią.
Stosowanie u dzieci
Nie są obecnie dostępne wystarczające dane potwierdzające stosowanie produktu Alfenta u dzieci w wieku poniżej 12 lat.
Działania niepożądane
Najczęściej występującymi działaniami niepożądanymi opioidów są depresja oddechowa i sztywność mięśni szkieletowych, szczególnie mięśni tułowia. Alfenta może powodować sztywność mięśniową obejmującą mięśnie szkieletowe szyi i kończyn. Postępowanie w przypadku depresji oddechowej i sztywności mięśni szkieletowych, patrz punkt FARMAKOLOGIA KLINICZNA, OSTRZEŻENIA i PRZECIWWSKAZANIA.
Profil działań niepożądanych z udziałem 696 pacjentów otrzymujących produkt Alfenta w ramach monitorowanej opieki anestezjologicznej (MAC) jest podobny do profilu ustalonego dla produktu Alfenta podczas znieczulenia ogólnego. Zdarzenia oddechowe zgłaszane podczas MAC obejmowały hipoksję, bezdechy i bradypneę. Inne zdarzenia niepożądane zgłaszane przez pacjentów otrzymujących produkt Alfenta w MAC, w kolejności malejącej częstości, to nudności, niedociśnienie, wymioty, świąd, splątanie, senność i pobudzenie.
Następujące informacje dotyczące działań niepożądanych pochodzą z kontrolowanych i otwartych badań klinicznych z udziałem 785 pacjentów, którym podawano dożylnie produkt Alfenta podczas indukcji i podtrzymywania znieczulenia ogólnego. Badania kontrolowane obejmowały porównanie leczenia z fentanylem, tiopentalem sodowym, enfluranem, placebo z solą fizjologiczną i halotanem. Na częstość występowania niektórych działań niepożądanych wpływa rodzaj zastosowania, np. sztywność ścian klatki piersiowej jest zgłaszana z większą częstością w badaniach klinicznych dotyczących indukcji znieczulenia za pomocą alfentanylu, oraz rodzaj zabiegu chirurgicznego, np. nudności i wymioty są zgłaszane z większą częstością u pacjentów poddawanych zabiegom ginekologicznym. Ogólne doniesienia o występowaniu nudności i wymiotów podczas stosowania produktu Alfenta były porównywalne z fentanylem.
Występowanie większe niż 1% – prawdopodobnie związane z przyczyną (pochodzące z badań klinicznych)
| * Częstość występowania 3% do 9% Wszystkie inne 1% do 3% |
|
| Żołądkowo-jelitowe: | nudności (28%), wymioty (18%) |
| Sercowo-naczyniowe: | arytmia, bradykardia (14%), nadciśnienie tętnicze (18%), nadciśnienie tętnicze (10%), tachykardia (12%) |
| Mięśniowo-szkieletowe: | sztywność ściany klatki piersiowej (17%), ruchy mięśni szkieletowych* |
| Oddechowe: | apnea*, pooperacyjna depresja oddechowa |
| Centralny układ nerwowy: | niewyraźne widzenie, zawroty głowy*, senność/ sedacja pooperacyjna |
Występowanie Mniej niż 1% – Prawdopodobnie związane przyczynowo (Uzyskane z badań klinicznych)
Zdarzenia niepożądane zgłoszone w ramach nadzoru po wprowadzeniu produktu do obrotu, niewystępujące w badaniach klinicznych, są wyróżnione kursywą.
| * Częstość występowania 0.3% do 1% | |
| Ciało jako całość: | anafilaksja |
| Centralny układ nerwowy: | ból głowy*, ruchy miokloniczne, dezorientacja pooperacyjna*, euforia pooperacyjna*, dreszcze* |
| Dermatologiczne: | swędzenie*, pokrzywka* |
| Miejsce wstrzyknięcia: | ból* |
| Mięśniowo-szkieletowe: | sztywność mięśni szkieletowych szyi i kończyn |
| Oddechowe: | skurcz oskrzeli, hiperkarbia*, skurcz krtani* |
Nadużywanie i uzależnienie od leków
Alfenta (chlorowodorek alfentanilu) jest substancją kontrolowaną z listy II, która może powodować uzależnienie od leków typu morfiny i dlatego może być potencjalnie nadużywana.
Opioidowe leki przeciwbólowe były związane z nadużywaniem i uzależnieniem u pracowników służby zdrowia i innych osób mających łatwy dostęp do takich leków. Alfenta powinna być odpowiednio traktowana.
Przedawkowanie
Przedawkowanie przejawiałoby się rozszerzeniem działań farmakologicznych produktu Alfenta (Alfentanilu chlorowodorek) (patrz FARMAKOLOGIA KLINICZNA), tak jak w przypadku innych silnych opioidowych leków przeciwbólowych. Podczas badań klinicznych nie odnotowano przypadków przedawkowania produktu Alfenta. Dożylna wartość LD50 produktu Alfenta wynosi 43-51 mg/kg u szczurów, 72-74 mg/kg u myszy, 72-82 mg/kg u świnek morskich i 60-88 mg/kg u psów. Dożylne podanie antagonisty opioidowego, takiego jak nalokson, powinno być stosowane jako swoiste antidotum w celu opanowania depresji oddechowej.
Czas trwania depresji oddechowej po przedawkowaniu produktu Alfenta może być dłuższy niż czas działania antagonisty opioidowego. Podanie antagonisty opioidowego nie powinno wykluczać natychmiastowego udrożnienia dróg oddechowych, podania tlenu oraz wspomaganej lub kontrolowanej wentylacji, zgodnie ze wskazaniami dotyczącymi hipowentylacji lub bezdechu. Jeśli depresja oddechowa jest związana ze sztywnością mięśni, może być konieczne zastosowanie środka blokującego mięśnie nerwowe w celu ułatwienia wspomaganej lub kontrolowanej wentylacji. Dożylne podawanie płynów i środków wazoaktywnych może być wymagane w celu opanowania niestabilności hemodynamicznej.
Alfenta dawkowanie i podawanie
Dawkowanie produktu Alfenta (chlorowodorek alfentanilu) powinno być zindywidualizowane i miareczkowane do pożądanego działania u każdego pacjenta w zależności od masy ciała, stanu fizycznego, podstawowego stanu patologicznego, stosowania innych leków oraz rodzaju i czasu trwania zabiegu chirurgicznego i znieczulenia. U pacjentów otyłych (ponad 20% powyżej idealnej całkowitej masy ciała), dawkę produktu Alfenta należy ustalić na podstawie beztłuszczowej masy ciała. Dawkę produktu Alfenta należy zmniejszyć u pacjentów w podeszłym wieku lub osłabionych (patrz PRECAUTIONS).
Należy rutynowo monitorować objawy życiowe.
Patrz wytyczne dotyczące dawkowania produktu Alfenta: 1) we wstrzyknięciu dożylnym jako środek przeciwbólowy uzupełniający znieczulenie barbituranem/podtlenkiem azotu/tlenem w przypadku krótkich zabiegów chirurgicznych (przewidywany czas trwania poniżej jednej godziny); 2) we wlewie ciągłym jako podtrzymujący środek przeciwbólowy z podtlenkiem azotu/tlenem w przypadku ogólnych zabiegów chirurgicznych; oraz 3) we wstrzyknięciu dożylnym w dawkach znieczulających do indukcji znieczulenia do ogólnych zabiegów chirurgicznych o przewidywanym czasie trwania co najmniej 45 minut; oraz 4) we wstrzyknięciu dożylnym jako składnik analgetyczny w monitorowanej opiece anestezjologicznej (MAC).
| DAWKOWANIE POWINNO BYĆ ZINDYWIDUALIZOWANE I MIARECZKOWANE | |
|---|---|
| DO STOSOWANIA W TRAKCIE ANESTEZJI OGÓLNEJ | |
| SPONTANICZNA WENTYLACJA/ASYSTENTNA WENTYLACJA | Indukcja analgezji: 8-20 mcg/kg Podtrzymanie analgezji: 3-5 mcg/kg q 5-20 min lub 0.5 do 1 mcg/kg/min Dawka całkowita: 8-40 mcg/kg |
| ZASTOSOWANA LUB KONTROLOWANA WENTYLACJA | |
| Wstrzyknięcie nasilające (W celu osłabienia reakcji na laryngoskopię i intubację) |
Indukcja analgezji: 20-50 mcg/kg Podtrzymanie analgezji: 5-15 mcg/kg q 5-20 min Dawka całkowita: Do 75 mcg/kg |
| Ciągła infuzja (W celu zapewnienia tłumienia odpowiedzi na intubację i nacięcie) |
Częstotliwość infuzji jest zmienna i powinna być miareczkowana do pożądanego efektu klinicznego. SEE INFUSION DOSAGE GUIDELINES BELOW. Indukcja znieczulenia: 50-75 mcg/kg Podtrzymanie znieczulenia: 0,5 do 3 mcg/kg/min (średnia szybkość 1 do 1,5 mcg/kg/min) Dawka całkowita: Zależna od czasu trwania procedury |
| Indukcja znieczulenia | Indukcja znieczulenia: 130-245 mcg/kg Podtrzymanie znieczulenia: 0,5 do 1,5 mcg/kg/min lub znieczulenie ogólne Dawka całkowita: Zależna od czasu trwania procedury Przy tych dawkach należy spodziewać się sztywności pnia i należy zastosować środek zwiotczający mięśnie. Podawać powoli (w ciągu 3 minut). Stężenie środków wziewnych zmniejszone o 30-50% przez początkową godzinę. |
| MONITOROWANA OPIEKA ANESTEZJOLOGICZNA (MAC) (Dla pacjentów uspokojonych i reagujących, oddychających spontanicznie) |
Indukcja MAC: 3-8 mcg/kg Podtrzymanie MAC: 3-5 mcg/kg q 5-20 min lub 0.25 do 1 mcg/kg/min Dawka całkowita: 3-40 mcg/kg |
Infuzja ciągła: 0,5-3 mcg/kg/min podawana z podtlenkiem azotu/tlenem u pacjentów poddawanych zabiegom chirurgii ogólnej. Po podaniu dawki indukującej znieczulenie Alfentą, wymagania dotyczące szybkości infuzji są zmniejszone o 30-50% przez pierwszą godzinę podtrzymywania.
Zmiany parametrów życiowych wskazujące na reakcję na stres chirurgiczny lub osłabienie znieczulenia można kontrolować poprzez zwiększenie dawki Alfentanilu do maksymalnie 4 mcg/kg/min i (lub) podawanie dawek bolusowych wynoszących 7 mcg/kg. Jeśli zmiany nie są kontrolowane po podaniu trzech dawek bolusa w ciągu pięciu minut, należy zastosować barbituran, środek rozszerzający naczynia krwionośne i/lub środek wziewny. Szybkość infuzji należy zawsze zmniejszać w przypadku braku tych objawów, aż do wystąpienia pewnej odpowiedzi na stymulację chirurgiczną.
W odpowiedzi na objawy osłabienia znieczulenia w ciągu ostatnich 15 minut operacji, zamiast zwiększania szybkości infuzji, należy podać dawki bolusa 7 mcg/kg produktu Alfenta lub silnego środka wziewnego. Infuzję produktu Alfenta należy przerwać co najmniej 10-15 minut przed zakończeniem zabiegu chirurgicznego.
Stosowanie u dzieci
Dane kliniczne potwierdzające stosowanie produktu Alfenta u pacjentów w wieku poniżej 12 lat nie są obecnie dostępne. Dlatego nie zaleca się takiego stosowania.
Premedykacja
Wybór leków stosowanych przed znieczuleniem powinien być oparty na potrzebach indywidualnego pacjenta.
Środki blokujące przewodnictwo nerwowo-mięśniowe
Wybrany środek blokujący przewodnictwo nerwowo-mięśniowe powinien być zgodny ze stanem pacjenta, z uwzględnieniem działania hemodynamicznego danego środka zwiotczającego mięśnie oraz wymaganego stopnia zwiotczenia mięśni szkieletowych (patrz punkty FARMAKOLOGIA KLINICZNA, OSTRZEŻENIA i PRZECIWWSKAZANIA).
W przypadku pacjentów, którym podaje się znieczulające (indukcyjne) dawki produktu Alfenta, konieczne jest zapewnienie wykwalifikowanego personelu i odpowiednich urządzeń do postępowania w przypadku śródoperacyjnej i pooperacyjnej depresji oddechowej.
Patrz także punkty OSTRZEŻENIA i PRZECIWWSKAZANIA.
Do celów dokładnego podawania małych objętości produktu Alfenta zaleca się stosowanie strzykawki tuberkulinowej lub jej odpowiednika.
Zgodność fizyczną i chemiczną produktu Alfenta wykazano w roztworze z normalnym roztworem soli fizjologicznej, 5% dekstrozy w normalnym roztworze soli fizjologicznej, 5% dekstrozy w wodzie i Lactated Ringers. Badania kliniczne infuzji produktu Alfenta zostały przeprowadzone z produktem Alfenta rozcieńczonym do zakresu stężeń od 25 mcg/mL do 80 mcg/mL.
Jako przykład przygotowania produktu Alfenta do infuzji, 20 mL produktu Alfenta dodane do 230 mL rozcieńczalnika daje roztwór produktu Alfenta o stężeniu 40 mcg/mL.
Pozajelitowe produkty lecznicze powinny być sprawdzane wzrokowo pod kątem obecności cząstek stałych i przebarwień przed podaniem, o ile roztwór i pojemnik na to pozwalają.
BEZPIECZEŃSTWO I POSTĘPOWANIE
Alfenta (Alfentanilu chlorowodorek) jest dostarczana w indywidualnie zamkniętych postaciach dawkowania, które nie stwarzają znanego ryzyka dla pracowników służby zdrowia mających przypadkowy kontakt. Przypadkowe narażenie skórne na Alfentę powinno być leczone przez spłukanie dotkniętego miejsca wodą.
Chronić przed światłem. Przechowywanie: Przechowywać w temperaturze 20° do 25°C (68° do 77°F). .
How is Alfenta Supplied
Alfenta (Alfentanilu chlorowodorek) Injection do stosowania dożylnego. Każdy mL Zawiera: Substancję czynną: Alfentanil base 500 mcg. Substancje pomocnicze: Sodu chlorek 9 mg i WFI Q.S Alfenta Injection jest dostępna jako:
NDC 11098-060-02, 2 mL Ampułka w opakowaniach po 10
NDC 11098-060-05, 5 mL Ampułka w opakowaniach po 10
NDC 11098-060-10, 10 mL Ampułka w opakowaniach po 5
NDC 11098-060-20, 20 mL Ampułka w opakowaniach po 5
U.S. Patent No. 4,167,574
May 1995, November 1995
TAYLOR PHARMACEUTICALS
AN AKORN COMPANY
Decatur, IL 62522
AFA0N Rev. 06/05
| Alfenta Alfentanil hydrochloride injection |
|||||||||||||||||||||||||||||||
|
|||||||||||||||||||||||||||||||
|
|||||||||||||||||||||||||||||||
|
|||||||||||||||||||||||||||||||
|
|||||||||||||||||||||||||||||||
Etykieciarka -. TAYLOR PHARMACEUTICALS
.