Zobacz ostatnie artykuły
Abstract
Rozwarstwienie aorty jest najczęstszym ostrym stanem nagłym aorty. Wczesne rozpoznanie i leczenie są niezbędne dla poprawy rokowania. Zaleca się, aby pole skanowania obejmowało całą aortę i naczynia miednicy, co ułatwia określenie typu i rozległości rozwarstwienia. Przedstawiliśmy przypadek ostrego rozwarstwienia aorty w obrazie i pokazaliśmy najbardziej reprezentatywne wyniki TC.
Skróty
AAS: Acute aortic syndrome; IH: Intramural hematoma; AD: Aortic dissection; PU: Penetrujący wrzód; CT: Tomografia komputerowa; RESA: Registro español de sindrome aortico (hiszpański rejestr zespołu aortalnego)
Słowa kluczowe
rozwarstwienie aorty, ostry zespół aortalny, zatrzymanie krążenia, naczynie krwionośne, pneumatoza wrotna, intestinal ischemia
Historia
An 81-year-old woman presented in Accident & Emergency in Marina Baixa Hospital, Villajoyosa, Alicante,complaining of severe abdominal pain for last two previous days and hypotension. Na oddziale ratunkowym doszło do zatrzymania krążenia i była reanimowana. Pacjentka została wstępnie zdiagnozowana z powodu naczynia krwionośnego w osierdziu po wykonaniu badania eko-kardiologicznego i tomografii komputerowej, która została natychmiast wykonana w celu wykluczenia rozwarstwienia aorty. Pacjent zmarł 10 minut później.
Wprowadzenie
Ostre rozwarstwienie aorty jest spowodowane pęknięciem intimy, które powoduje przedostanie się krwi do ściany aorty oddzielającej warstwy środkowe, tworząc w ten sposób zdefiniowany fałszywy kanał pomiędzy zewnętrzną warstwą środkową i adventitią na zewnątrz a kompleksem intymnym, przyśrodkowym lub „klapą” wewnątrz. Nowo utworzony kanał wykazuje w swojej interwencji przepływ, który powraca dystalnie do światła naczynia przez otwór re-entry .
Dyssekcja aorty jest zaliczana do ostrego zespołu aortalnego (AAS), wraz z krwiakiem śródściennym i wrzodem penetrującym 1. Charakteryzują się one:
-Krwiak śródścienny (IH) jest krwotokiem, który dotyczy warstwy środkowej ściany aorty. To generuje rozdarcie vasa vasorum, które jest również znane jako rozwarstwienie aorty bez formowania płata śródściennego .
-Dyssekcja aorty (AD) jest rozdarciem wewnętrznej warstwy ściany aorty generującym formowanie płata śródściennego, co pozwala na przedostanie się krwi do ściany aorty, tworząc nowe przejście dla krwi zwane fałszywym światłem, odróżnione od prawdziwego światła (zwanego również kanałem aortalnym) przez płat.
-Penetrujący wrzód (PU) odnosi się do wrzodziejącej zmiany miażdżycowej, która penetruje elastyczną blaszkę i jest związana z tworzeniem krwiaka w obrębie mediów ściany aorty .
Dwie klasyfikacje są najczęściej używane do rozwarstwienia aorty. System DeBakey jest podzielony na trzy typy (typy I, II, i III) w zależności od lokalizacji pierwszego wejścia rozwarstwienia. Typ I charakteryzuje się pierwszym wejściem w aorcie wstępującej i rozprzestrzenia się dystalnie do aorty zstępującej. Typ II ma pierwsze wejście w aorcie wstępującej i nie rozprzestrzenia się do łuku aorty. Typ III ma pierwsze wejście w aorcie zstępującej i rozprzestrzenia się dystalnie powyżej (typ IIIa) lub poniżej (typ IIIb) przepony. System Stanforda jest podzielony na dwa typy (typ A i B) w zależności od zajęcia aorty wstępującej. Typ A obejmuje rozwarstwienie w aorcie wstępującej niezależnie od miejsca pierwszego wejścia. Typ B nie obejmuje rozwarstwienia aorty wstępującej .
Oszacowano, że w Hiszpanii AAS występuje z częstością 20-40 przypadków na milion mieszkańców rocznie i jest bardziej rozpowszechniony u mężczyzn (80%) niż u kobiet. Spośród podtypów AAS najczęściej występuje AD (80%), następnie IH (15%) i PU (5%). Jeśli chodzi o lokalizację pierwszego wejścia dyssekcji, 68% dotyczy aorty wstępującej (typ A), a 32% aorty zstępującej (typ B) .
Śmiertelność jest wysoka w typie A i wymaga pilnej operacji. Typ B wymaga leczenia przeciwnadciśnieniowego 1.
Rozwarstwienie aorty rozpoczyna się bólem w klatce piersiowej lub brzuchu, który promieniuje do pleców, symulując inne patologie. Do 20% chorych ma obraz synkopowy spowodowany tamponadą serca lub niedrożnością pni nadaortalnych. Ból brzucha pojawia się w wyniku uszkodzenia gałęzi brzusznych.
Wyniki badań obrazowych
Zgodnie z plikami RESA 6, tomografia komputerowa (CT) jest najczęściej stosowaną techniką obrazowania w diagnostyce pacjentów z podejrzeniem AD. Wielowarstwowa zdolność CT do rekonstrukcji obrazu pozwala na uzyskanie prawie 90% czułości i 85% swoistości .
Faza niewzmocniona
CT nie dostarcza informacji dynamicznych. Na przykład, nie dostarcza informacji ani o funkcji skurczowej lewej komory, ani o zachowaniu zastawki aortalnej, które są kluczowe dla rozróżnienia między krwiakiem śródmiąższowym a diagnozą rozwarstwienia aorty. Aby móc odróżnić krwiaka śródściennego od rozwarstwienia aorty w obecności aktywnego krwawienia, wskazane byłoby uzyskanie obrazów bez kontrastu, ponieważ są one klinicznie nierozróżnialne.
Jak widzimy na rycinach 1 i 2, nie można wykryć żadnych cech krwiaka śródściennego. Zamiast tego obserwujemy osierdziowe naczynie krwionośne uwidocznione wcześniej w echokardiogramie ratunkowym, które skłoniło nas do wykonania tomografii komputerowej. Możemy również zaobserwować płat aorty, wskazujący na rozwarstwienie.
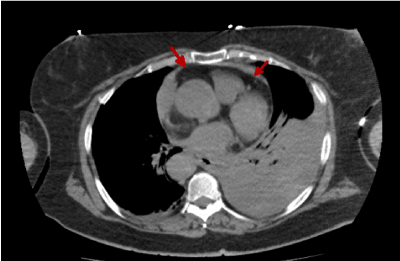
Ryc. 1. Obraz TK klatki piersiowej bez i.v.c. pokazujący osierdziowe naczynie krwionośne (czerwone strzałki)
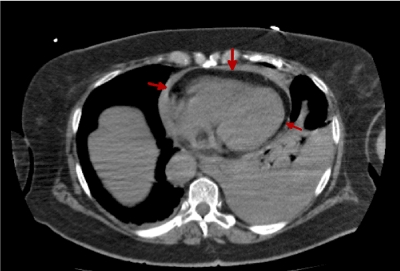
Rysunek 2. Obraz TK klatki piersiowej bez i.v.c. Widoczne naczynie krwionośne w bardziej ogonowym obrazie (czerwone strzałki)
Faza tętnicza
Sekwencje tomografii komputerowej są wykonywane z dożylnym podaniem kontrastu. Celem tego jest ocena morfologii kanału aorty, prawdziwego światła i możliwość obserwacji nowych przejść krwi do fałszywego światła.
Zastosowany protokół obejmuje całą aortę i jej główne odgałęzienia, od tętnicy podobojczykowej do początku tętnicy udowej.
Na rycinie 3 możemy wyraźnie zaobserwować płatek aorty i to, jak dzieli on trajektorię krwi w kanale aortalnym (czerwona strzałka).
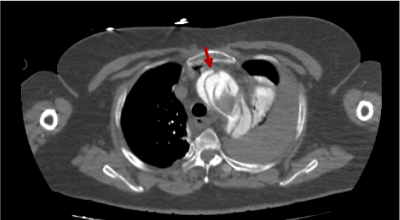
Figura 3. Obraz TK klatki piersiowej z i.v.c. w fazie tętniczej, na którym obserwujemy rozwarstwienie aorty typu A (czerwona strzałka)
Rysunek 4, przedstawia dodatkowe informacje. Należą do nich: (i) hipointensywny płat aortalny obecny w aorcie zstępującej (zielona strzałka); (ii) rozwarstwienie całej intimy pozwala nam zaobserwować obwodowy płat intymny i wąskie światło prawdziwe w kształcie nitkowatym (zielona strzałka)7; (iii) czerwona strzałka pokazuje również typowy rozkład objawu pajęczyny. Pojawienie się tego rozkładu jest wyraźną oznaką fałszywego światła; (iv) hiperintensywna tętnica płucna (niebieska strzałka).
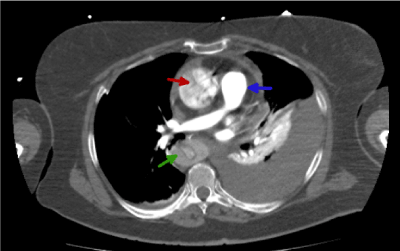
Ryc. 4. Obraz TK klatki piersiowej z i.v.c. w fazie tętniczej, który pokazuje rozwarstwienie i fałszywe światło (zielona strzałka)
Podążając kanałem aortalnym docieramy do aorty brzusznej:
Rysunki 4 i 5 pokazują nieruchomy płat aorty na poziomie brzucha (czerwona strzałka). Jest to efekt rozwarstwienia i pomimo dożylnego podania kontrastu widzimy, że kanał aorty jest hipointensywnie wzmocniony. Jednak obserwujemy obie żyły wątrobowe i żyły nerkowe jako hiper-enhanced (zielona strzałka), kiedy, teoretycznie, żylny przepływ przychodzi po tętniczym przepływie, w późnej fazie .
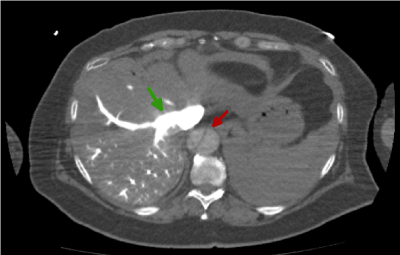
Figure 5. Obraz TK jamy brzusznej z i.v.c. w fazie tętniczej, który pokazuje dyssekcję na poziomie brzucha(czerwona strzałka)
Dodatkowo widać, że kontrast ma tendencję do gromadzenia się w części grzbietowej ciała (niebieska strzałka). Ryciny 5 i 6 pokazują wątrobę bez kontrastu w obszarze brzusznym. Zamiast tego kontrast ma tendencję do gromadzenia się w obszarze grzbietowym. To nieregularne rozmieszczenie kontrastu dożylnego jest również zgodne ze wspomnianą wcześniej ideą asystolicznego pompowania krwi.
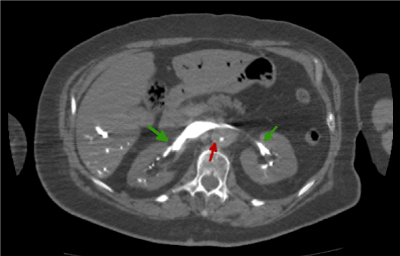
Ryc. 6. Obraz TK jamy brzusznej z i.v.c. w fazie tętniczej, na którym obserwujemy hiper-wzmocnione żyły nerkowe
Gdy dochodzi do zatrzymania krążenia, przepływ krwi zwalnia, ciśnienie krwi i żylne gwałtownie spada do niewykrywalnych poziomów, a normalne gradienty ciśnień między różnymi układami naczyniowymi zostają utracone. Dlatego dystrybucja wstrzykniętego w tym czasie środka kontrastowego będzie zdeterminowana przez ciśnienie wytworzone przez pompę iniekcyjną oraz przez ciśnienie hydrostatyczne.
W ten sposób wymuszony refluks kontrastu gromadzi się w obszarach schyłkowych prawej części ciała, szczególnie w strukturach żylnych jamy brzusznej (żyła główna dolna, żyły wątrobowe i nerkowe) (ryc. 5-8), a także w miąższu wątroby (prawy płat wątroby) i obszarze nerek. Ponieważ kontrast nie ulega rozcieńczeniu z krwią krążącą, obserwuje się wyraźne zagęszczenie tych struktur. W miarę spowalniania przepływu krwi, dyssekcja
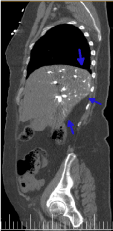
Ryc. 7. Rekonstrukcja w płaszczyźnie strzałkowej obrazu TK klatki piersiowej i jamy brzusznej z i.v.c. w fazie tętniczej. Widoczne gromadzenie się kontrastu w części grzbietowej ciała (niebieska strzałka).
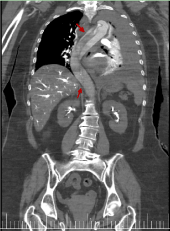
Rys. 8. Obraz rekonstrukcji koronalnej z TK klatki piersiowej-brzucha z i.v.c. w fazie tętniczej. Widać na nim płat aorty w całej trajektorii aortalnej (czerwona strzałka)
w fazie wrotnej jest lepiej uwidoczniony .
Rysunek 9 pokazuje wewnętrzne przemieszczenie zwapnień intymnych.
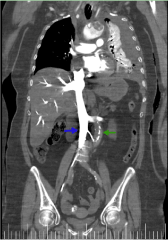
Rysunek 9. Obraz rekonstrukcji koronalnej z TK klatki piersiowej i jamy brzusznej z i.v.c. w fazie tętniczej.Pokazuje różnicę wzmocnienia między aortą brzuszną (zielona strzałka) a żyłą główną dolną (niebieska strzałka)
Faza późna
Ze względu na nieregularne rozmieszczenie kontrastu dożylnego, zdecydowaliśmy się wykonać sekwencję późną, która odpowiada fazie wrotnej.
Różnice wzmocnienia między fazami pokazane są na rycinach 10-13. Płatek jest widoczny na obu obrazach, ale jest lepiej uwidoczniony w fazie wrotnej.
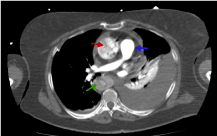
Ryc. 10. Obraz TK klatki piersiowej z i.v.c. w fazie tętniczej, gdzie wyróżniamy różne wzmocnienia
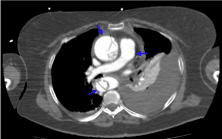
Rycina 11. Ten sam obraz co na rycinie 10, ale w późnej fazie wrotnej. Widać, jak wzmocnienia zostały zrównoważone w każdej strefie (niebieska strzałka)
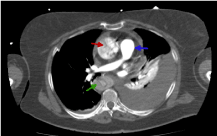
Rysunek 12. Obraz TK jamy brzusznej z i.v.c. w fazie tętniczej, na którym obserwujemy hipowzmocnioną aortę brzuszną
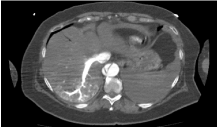
Rysunek 13. Ten sam obraz co na rycinie 12, ale z i.v.c. w późnej fazie wrotnej. Widzimy teraz wzmocnienie aorty jest przy tej samej intensywności jak ten w żyle porta
Rysunek 14 pokazuje , że płaty są jeszcze obecne na końcu aorty, tuż przed rozwidleniem aorty.
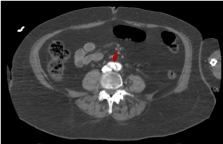
Rysunek 14. Obraz TK jamy brzusznej z i.v.c. w późnej fazie wrotnej, który pokazuje, jak dyssekcja trwa do samego końca tętnicy aortalnej (czerwona strzałka)
Jednakże rycina 15 pokazuje trajektorię w dół płata bezpośrednio po rozwidleniu płata wewnątrz prawej tętnicy biodrowej wspólnej. Możemy zatem potwierdzić, że rozwarstwienie aorty u tego pacjenta jest kompletne i obejmuje całą trajektorię tętnicy aortalnej, od odcinka wstępującego do rozwidlenia aorty, a nawet dalej w prawej tętnicy biodrowej wspólnej.
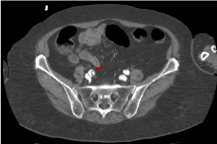
Ryc. 15. Obraz TK jamy brzusznej z i.v.c. w późnej fazie wrotnej, na którym widać, że rozwarstwienie aorty dotarło nawet do prawej tętnicy biodrowej wspólnej (czerwona strzałka)
Na rycinach 16 i 17 widzimy prawie całą trajektorię rozwarstwienia aorty, łącznie z tętnicami biodrowymi wspólnymi.
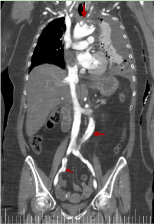
Rycina 16. Rekonstrukcja koronalna z TK klatki piersiowej-brzucha z i.v.c. w późnej fazie wrotnej, która pokazuje zasięg rozwarstwienia aorty (czerwona strzałka)
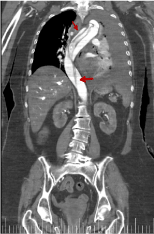
Rysunek 17. Rekonstrukcja koronalna z TK klatki piersiowej i jamy brzusznej z i.v.c. w późnej fazie wrotnej, która pokazuje zasięg rozwarstwienia aorty (czerwona strzałka)
Rysunki ogólne
Rysunki 18-22 przedstawiają powietrze w układzie wrotnym. Jego główną etiologią jest niedokrwienie jelit. Jest to powszechnie uważane za predyktor perforacji jelita i może prowadzić do błędnego rokowania. W opisywanym przypadku pneumatoza wrotna sugeruje niedokrwienie jelit z powodu niskiego rzutu serca w następstwie niewydolności aortalnej, przebytego zatrzymania krążenia i/lub zajęcia gałęzi tętnic brzusznych przez rozwarstwienie. Ból brzucha prezentowany przez naszego pacjenta może być spowodowany niedokrwieniem jelit .
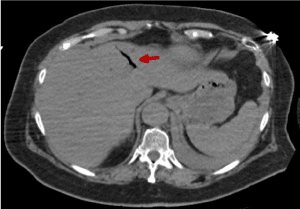
Rysunek 18. Obraz TK jamy brzusznej, który pokazuje obecność powietrza w układzie wrotnym (czerwona strzałka)
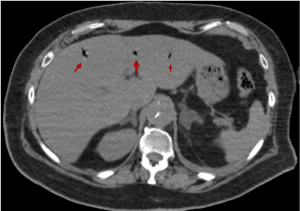
Rysunek 19. Obraz TK jamy brzusznej wykazujący obecność powietrza w układzie wrotnym (czerwona strzałka)
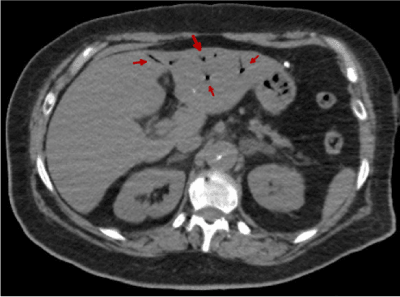
Ryc. 20. Obraz TK jamy brzusznej wykazujący obecność powietrza w układzie wrotnym (czerwona strzałka)
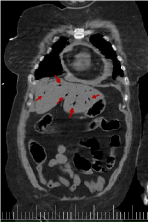
Rys. 21. Rekonstrukcja koronowa z tomografii komputerowej z obecnością powietrza w układzie wrotnym (czerwona strzałka)
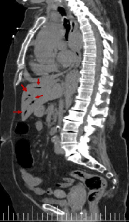
Rysunek 22. Sagittal reconstruction from CT scan with air presence in portal system(red arrow)
Wnioski
Dyssekcja aorty jest najczęstszą przyczyną nagłych przypadków aorty i jako taka powinna być zawsze podejrzewana w takich sytuacjach. Jak wykazano w niniejszym opisie przypadku, aby uniknąć w przyszłości zgonów, którym można zapobiec, należy je pilnie zdiagnozować i leczyć. W celu właściwego rozpoznania rozwarstwienia aorty zalecamy wykonanie tomografii komputerowej z następującymi sekwencjami: (i) Faza bez wzmocnienia, w celu zróżnicowania pomiędzy IH i AD; (ii) Faza tętnicza z kontrastem dożylnym; (iii) Faza późna z kontrastem dożylnym dopasowanym do fazy wrotnej; (iv)
- Michelle A. McMahon, FRCR, Christopher A (2010) Multidetector CT of aortic dissection: A pictorial review. Squirrell, FRCR; Radiographics 30(2):445-460.
- Ihab B, Alomari Yasmin S, Hamirani George Madera, Cyril TabeNila Akhtar, Veena Raizada (2014) Aortic intramural hematoma and its complications. Circulation 129:711-716.
- Derek Juang, Alan C Braverman, Kim Eagle (2008) Aortic Dissection. Circulation 118:e507-e510.
- Hideyuki Hayashi, Yohjiro Matsuoka, Ichiro Sakamoto, Eijun Sueyoshi, Tomoaki Okimoto, et al. (2000) Penetrating atherosclerotic ulcer of the aorta: Imaging features and disease concept. RadioGraphics 20:995-1005.
- Fukui T (2018) Management of acute aortic dissection and thoracic aortic rupture. Journal of Intensive Care 6(15).
- A Evangelista, F Padilla, J López-Ayerbe, F Calvo, JM López-Pérez, et al. (2009) Segun datos del Registro Español de SAA (RESA). Rev Esp Cardiol 62(3):255-262.
- Szpitale uczestniczące w hiszpańskim badaniu ostrego zespołu aortalnego. Spanish Acute Aortic Syndrome Study (RESA). Better Diagnosis Is Not Reflected in Reduced Mortality. Rev Esp Cardiol (Engl Ed) 62:255-262.
- Hallinan JTPD, Anil G (2014) Multi-detector computed tomography in the diagnosis and management of acute aortic syndromes. World Journal of Radiology 6(6):355-365.
- Consenso de Patologia de la Aorta. Revista Argentina de Cardiología. 2014; Volumen 72 n.º 5. Septiembre-Octubre 393.
- Bae KT (2010) Intravenous contrast medium administration and scan timing at CT: Considerations and Approaches. Radiology 256.
- Ko Sheung-Fat, Ng Shu-Hang, Chen Min-Chi, Lee Tze-Yu, Huang Chung-Cheng, et al. Sudden cardiac arrest during computed tomography examination: Clinical finding and „Dense Abdominal Veins” on computed tomography. Journal of Computer Assisted Tomography 27(1):93-97.
- Laura Morales C, Jorge Carrillo B, Juan Sebastián Ojeda G, Germán Torres A (2018) Portograma aéreo y neumatosis intestinal como hallazgos incidentales en postoperatorio de cirugía abdominal. Revista Chilena de Radiología 24;40-43.
- Mario ML, Andrés GM, Carmen NR, Susana PB, Soliveres S (2014) Neumatosis portomesentérica e intestinal: no siempre es lo que parece. Acta Gastroenterológica Latinoamericana 44(3):246-251.
- Reoyo-Pascual JF, León-Miranda R, Valero-Cerrato X, Rosa M (2013) Portal pneumatosis: sign of alert or casual discovery? Revista española de enfermedades digestivas 105(5).
.