Amfetamin | Missbrukssjukdomar
Ampetaminets ursprung
Ampetamin syntetiserades för första gången 1887 av L. Edelano. År 1920 upptäckte Gordon Alles att moderföreningen amfetaminsulfat och dess ännu mer aktiva dextroisomer, dextroamfetaminsulfat, hade förmågan att stimulera det centrala nervsystemet (CNS). År 1931 började läkemedelslaboratorier i USA studera det, och fem år senare, under förbudstiden, introducerade Smith Kline & French, det läkemedelsföretag som hade förvärvat Alles patent, det i den medicinska praktiken under handelsnamnet Benzedrine® (bennies för stamgästerna). Nästan omedelbart kom dess mer aktiva isomer, dextroamfetamin som marknadsförs som Dexedrine® (dexies), på marknaden. Efter att båda typerna av amfetamin hade införts i förteckningarna över kontrollerade substanser dök de upp på den svarta marknaden i Nordamerika under namn som var relaterade till deras subjektiva effekter, t.ex. speed och uppers.
Struktur och klassificering
Ampetaminer är sympathomimetiska aminer med en strukturell kemisk formel som liknar adrenalin (fig. 1). De två vanligaste amfetaminerna, från vilka de modernaste drogerna i denna grupp härstammar, är d-amfetaminsulfat eller d-fenylisopropylamin (dexedrin), som motsvarar den dextrorotatoriska isomeren av denna substans, och racemiskt amfetaminsulfat (bensedrin) (fig. 2). Den dextrorotatoriska föreningen (dexedrin eller d-benzedrin) är dubbelt så aktiv som den racemiska föreningen (bensedrin) och fyra gånger så aktiv som den levorotatoriska föreningen. Farmakologiskt sett, när en förening med en adrenalinliknande kemisk struktur rör sig bort från adrenalin och övergår till amfetamin, ökar dess CNS-stimulerande aktivitet och minskar dess aktivitet i kroppens periferi (neurovegetativa system).
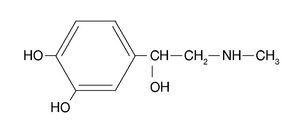
Figur 1. Kemisk struktur för adrenalin.
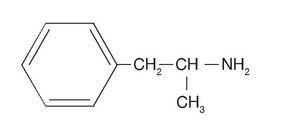
Figur 2. Kemisk struktur för dl-amfetamin.
De vanligaste psykostimulerande preparaten av amfetamin är amfetamin, fentermin, klorfentermin och metamfetamin (fig. 3), varav det sistnämnda är av stor betydelse eftersom det ligger till grund för MDMA-gruppen (3,4-metylendioxymetamfetamin; ecstasy). Ett antal föreningar som tillhör gruppen heterocykliska aminer som inte är amfetamin och som framställs av piperdinättiksyra har också dykt upp, t.ex. metylfenidat och pripadol. Andra heterocykliska aminer är phacetoteran och fenmentracin. Dessa läkemedel är relativt nya, även om växten som efedrinet kommer ifrån (Catha edulis) har använts sedan urminnes tider för behandling av astma. Från och med 1960-talet och framåt gjorde reklamen amfetaminanvändningen återigen populär på grund av dess aptitdämpande (anorektiska) egenskaper.
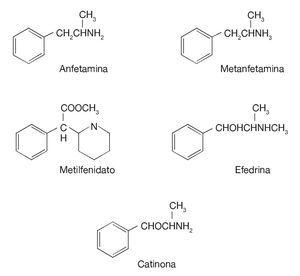
Figur 3. Kemisk struktur för amfetamin och vissa derivat.
Ansvarsmekanismer
Ampetaminer har en verkningsmekanism som involverar flera neurotransmittorer som dopamin, serotonin, adrenalin och noradrenalin.
Ökad frisättning av dopamin
Den ökade koncentrationen av neurotransmittorn i det synaptiska utrymmet uppstår både genom att blockera återupptaget, i en mekanism som liknar kokainets men med en annan fixeringspunkt, och genom ökad frisättning, eftersom d-amfetamin kan tränga in i neuronet och förflytta dopamin från dess icke-granulära cytoplasmatiska lager (fig. 4), med efterföljande utarmning av neurotransmittorer1,2.
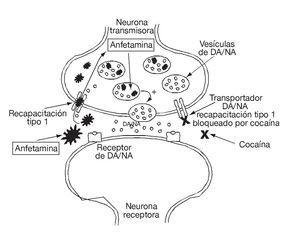
Figur 4. Schematisk bild av amfetaminers verkningsmekanism på de dopaminerga och noradrenerga neurotransmittorsystemen. DA: dopamin; NA: noradrenalin.
Denna ökning av dopamin i områden i den laterala hypotalamus reglerar dosberoende aptitkänslan. Förhöjda dopaminnivåer i de nigrostriatala och mesokortikolimbiska banorna (fig. 5) har varit inblandade i de psykostimulerande och belönande egenskaperna hos amfetamin.
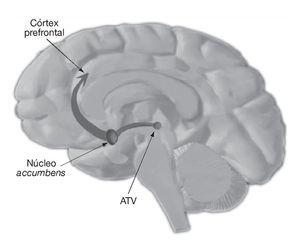
Figur 5. VTA: ventral tegmental area.
Hämning av serotoninåterupptag
Ampetamin ökar de extracellulära koncentrationerna av serotonin3 genom att neurotransmittorn förskjuts från sin specifika presynaptiska transportör. När amfetamin binder till serotonintransportörer hindrar det både serotonin från att komma in i terminalen och vänder återupptagsmekanismen så att serotonin kommer ut i det synaptiska utrymmet. Denna mekanism verkar mer selektiv för läkemedel som fenfluramin och dexfenfluramin, som också frigör serotonin från sina intracellulära lager och kan aktivera 5-HT1-receptorer. Ökat serotonin är också inblandat i den anorektiska effekt som amfetamin ger.
Ökat frisättande av noradrenalin
Ampetaminer underlättar frisättandet av noradrenalin genom att transporteras till nervändarna genom återupptagsmekanismen (fig. 4). När de når nervändarna tas de upp av den vesikulära transportören i utbyte mot noradrenalin, som försvinner till cytosolen. De verkar endast svagt på adrenergiska receptorer. Denna mekanism skulle delvis förklara de centrala effekterna av amfetamin, t.ex. ökad motorisk aktivitet och minskad trötthet, och de perifera effekter som följer med dessa läkemedel, t.ex. takykardi, svettning och svårigheter att urinera.
Störning av den vesikulära monoamintransportören
Den vesikulära monoamintransportören (VMAT2) finns huvudsakligen i CNS och ansvarar för transporten av monoaminer som finns i cytoplasman till lagringsvesiklar. Amfetamin kan störa protongradienten i membranen hos dessa synaptiska vesiklar och därmed deras funktion. De vänder därmed flödet av dessa transportörer, vilket leder till ökade cytoplasmatiska koncentrationer av noradrenalin, dopamin och serotonin. Eftersom VMAT2 kan spela en roll i den lokomotoriska stimuleringen och de förstärkande egenskaperna hos amfetamin kan det vara ett mål för utveckling av terapeutiska strategier för beroendeframkallande processer i samband med användning av psykostimulerande medel4.
Farmakologiska effekter av amfetamin
Perifert
Ampetamin ger upphov till perifer vasokonstriktion och därmed en ökning av både systoliskt och diastoliskt blodtryck. Det ökar hjärtfrekvensen genom beta-adrenerg verkan, även om den också kan minska reflexmässigt. På glattmuskelnivå drar den ihop den radiella muskeln i iris, vilket leder till mydriasis och ökat intraokulärt tryck. Peristaltiken minskar, liksom sekretet. Avslappnar bronkialmuskulaturen genom beta-adrenergisk verkan. Det drar ihop blåsans slutmuskel, vilket försvårar urinering.
På centralnervsnivå
Ampetamin ger en känsla av vakenhet, stimulans, förbättrad intellektuell prestation och utförandet av manuella uppgifter, en känsla av energi, minskad trötthet, sömn och hunger. De har en hög risk för missbruk och kan orsaka beroende. Hos försöksdjur ger amfetamin en dosberoende ökning av den lokomotoriska aktiviteten, och vid höga doser ger de upphov till stereotypier. Det har föreslagits att binge eating hos människor kan vara en manifestation av stereotypt beteende hos djur.
Tolerans
Både subjektiva och objektiva effekter genomgår fenomenet tolerans efter upprepad användning av amfetamin och derivat av amfetamin, så att högre doser krävs för att uppnå samma effekt.
Denna tolerans kan vara kronisk eller akut (takyfylaxi). Den föreslagna mekanismen för tolerans eller desensibilisering inbegriper receptorfosforylering som leder till en frikoppling mellan G-proteinet och själva receptorn5. Både kronisk och akut tolerans är delvis ansvariga för tendensen att missbruka amfetaminderivat i jakt på stimulerande effekter. Tachyfylaxi kan däremot leda till livshotande överdosering. Kors-tolerans mellan sympatomimetiska medel av amfetamintyp har observerats kliniskt, och kors-tolerans mellan den anorexiska effekten av kokain och amfetamin har påvisats hos råttor. Dessutom har man beskrivit omvänd tolerans eller sensibilisering, som är karakteristisk för användning av amfetaminderivat och som yttrar sig i form av överdosering efter intag av vanliga doser.
Sensibilisering
En beteendekänslighet avser den ökade responsen på amfetamin efter upprepad administrering. Det ventrala tegmentala området (VTA) har involverats i framkallandet av amfetaminmedierad beteendekänslighet6. Sensibiliseringen beror förmodligen på en desensibilisering av presynaptiska D2-dopaminerga receptorer, som negativt modulerar dopaminfrisättningen i vissa hjärnområden, t.ex. i nucleus accumbens. Administrering av läkemedlet kommer således att resultera i en ytterligare ökning av synaptiskt dopamin, med en följdriktig ökning av effektens intensitet. Sensibiliseringen kan vara långvarig och verkar utvecklas snabbare när läkemedlet ges intermittent. Nyligen har en annan mekanism beskrivits som försöker förklara sensibilisering. Amfetamin (d-amfetamin och fenfluramin) kan således utnyttja den presynaptiska transportören för serotonin genom att förskjuta den, vilket förhindrar fosforylering som leder till intracellulär distribution av serotonin och ökar antalet transportörer som är tillgängliga i membranet för efterföljande doser av läkemedel. Denna omfördelning av återupptagsproteiner i membranen kan representera några av de molekylära förändringar som är inblandade i känslighet för stimulerande effekter. Detta fenomen tros vara orsaken till de psykotiska tillstånd som ibland följer med användningen av dessa droger.
Beroende
Ampetaminer tas till en början i enstaka doser och ger upphov till eufori och förstärkning (startfasen), främst på grund av deras förmåga att frisätta dopamin vid dopaminerga terminaler i den mesokortikolimbiska banan (nucleus accumbens och prefrontal cortex). När konsumtionen ökar (konsolideringsfasen) utvecklas en tolerans som kan övervinnas genom att öka dosen eller ändra administreringsvägen. I detta skede börjar dopaminförbrukningen. Tolerans byggs upp och man börjar äta för att bibehålla euforin. Den stora suget varar i 12-48 timmar och slutar med att personen är utmattad och behöver flera dagar för att återhämta sig. I denna fas är dopaminnivåerna mycket låga och neuronala skador kan förekomma.
De allmänna kriterierna för missbruk (mindre frekvent användning än beroende) i Diagnostic and Statistical Manual of Mental Disorders IV (DSM-IV) gäller för amfetamin och syntetiska droger. De observeras som icke-kompatibla, använder i riskfyllda situationer och kan ha juridiska, sociala och interpersonella problem på grund av sitt bruk och dess konsekvenser.
DSM-IV:s allmänna kriterier för amfetaminberoende gäller också för amfetamin. Amfetaminberoende åtföljs av intensiv tolerans, tillbakadragande och tillbakadragande från vanliga aktiviteter. Ett oemotståndligt behov av att använda (craving) utvecklas. Psykotiska symtom uppträder ofta vid användning. När man plötsligt slutar med kronisk amfetaminanvändning uppstår ett abstinenssyndrom med olika faser. Den första fasen (kraschen) börjar inom några timmar och varar upp till nio dagar. Dysphori, depression, anergi, agitation, ångest, sömnlöshet, hypersomnolens, hyperfagi och intensivt sug uppträder. Den mellanliggande fasen eller abstinensfasen inträffar mellan 1 och 10 veckor. Initialt visar den sig i form av trötthet, energilöshet, anhedoni och depression. Suget minskar och om det inte blir något återfall förbättras de depressiva symtomen gradvis. I den tredje fasen, som är obestämd, kan intensiva episoder av sug uppträda, vanligtvis relaterade till betingade signaler, vilket kan leda till att patienten får ett återfall. Hos personer som har tagit stora doser kan självmordstankar förekomma. En liknande bild har beskrivits för kokain. Det finns ingen specifik farmakologisk behandling för amfetaminberoende. Eftersom det verkar som om dopaminet kan minska under abstinenserna har dopaminagonister och antidepressiva läkemedel använts. Resultaten med psykofarmaka är nedslående. Psykoterapi kan vara till hjälp. Amfetamininducerade störningar behandlas symtomatiskt, antipsykotika för psykotiska manifestationer och anxiolytika för ångest och panikattacker eller ångestsyndrom. De farmakologiska effekterna av metamfetamin har nyligen granskats7.
Neurotoxicitet av metamfetamin
Neurotoxicitet orsakad av substanser definieras som en skadlig strukturell eller funktionell förändring i CNS. Neurotoxicitet orsakad av amfetamin avser således vanligtvis bestående förändringar på neurokemisk och neuronal nivå, inklusive skador på axoner och monoaminhaltiga ändar. Hos råttor och apor leder administrering av metamfetamin till en minskning av dopamin och dess metaboliter8. Hos råttor minskar metamfetamin också serotoninnivåerna, dopamin- och serotoninåterupptagningsställena, minskar aktiviteten hos enzymer som är involverade i neurotransmittorsyntesen (tyrosinhydroxylas och/eller tryptofanhydroxylas) och ger upphov till morfologiska förändringar i neuronerna9. Strukturella förändringar i neuronerna observeras i axonerna och inkluderar uppkomsten av varicositeter och en minskning och utarmning av axonerna. Faktorer som påverkar utvecklingen av neurotoxicitet hos metamfetamin är bland annat de doser som används, antalet exponeringar för läkemedlet, intervallet mellan doserna och hur länge neuronerna utsätts för läkemedlet. Även om uppgifterna om människor är mycket begränsade visar vissa studier att metamfetamin hos människor kan ge bestående dopaminerga neurotoxicitet i samband med funktionsförändringar, men en viss regenerering av de drabbade neuronerna har också observerats flera månader efter att man slutat använda drogen10.
Neurobiologiska studier på försöksdjur
Effekter på lokomotorisk aktivitet
Ampetaminer ger central stimulering11 , en term som används för att beskriva deras effekter på den lokomotoriska aktiviteten hos djur och på sömn och elektroencefalografisk aktivitet. Initialt framkallar amfetamin ett tillstånd av vakenhet som åtföljs av en ökning av utforskande beteende, putsning, vertikal och horisontell rörelse, följt av en minskning av dessa aktiviteter till förmån för stereotypa beteenden (omvänt U-formad dosrespons). Neuroanatomiska studier visar att den ökning av den lokomotoriska aktiviteten som amfetamin ger upphov till är beroende av det nigrostriatala och mesolimbiska dopaminerga systemet. Dessutom kan den centrala frisättningen av noradrenalin vara viktig för hyperlocomotion. Å andra sidan verkar stereotypier förmedlas av frisättning av nysyntetiserat dopamin i de nigrostriatala och mesolimbiska dopaminerga vägarna och regleras av en balans mellan de dopaminerga och kolinerga systemen.
Effekter på aggressivt beteende
Amfetamins effekter på aggressivt beteende hos djur är komplexa och beror på dosen som administreras och det experimentella paradigm som används. Miljöfaktorernas och de genetiska faktorernas roll för dessa effekter är också viktig. Hos både djur och människor kan amfetamin ge upphov till extrema aggressioner och till att man drar sig tillbaka från allt socialt utbyte. De neurobiologiska mekanismer som är inblandade i amfetaminets många olika effekter på aggressivt beteende har kopplats till de mekanismer som är relevanta för dess psykostimulerande egenskaper. Ett av de paradigmer som används för att studera effekterna av dessa ämnen på aggressivt beteende är inkräktartestet. Testet innebär konfrontationer mellan ett inhemsk djur och en inkräktare och undersöker biologiskt giltiga beteenden som underkastelse, försvarsbeteende, attack och flykt. Amfetamin har således visat sig öka försvars- och flyktbeteendet under olika experimentella förhållanden och hos olika djurarter, och denna effekt verkar inte förmedlas av det centrala dopaminerga systemet. Dopaminantagonister vänder dock de förstärkande effekterna av aggressivt beteende vid akut administrering av låga doser amfetamin.12
Effekter på inlärning
De flesta djurstudier tyder på att amfetamin inte stör inlärningen, och under vissa förhållanden kan det till och med förstärka den. Det finns dock även uppgifter som visar på skadliga effekter13. Det är väl etablerat att inlärning med amfetamin är bättre ihågkommen om man ger amfetamin i stället för saltlösning samma dag som testet genomförs. Under amfetaminavvänjning uppträder dessutom störningar i det beteende som man lärt sig under amfetaminets påverkan. Det har alltså visats att det inre tillstånd som amfetaminet ger upphov till hos djuret påverkar inlärningen av uppgifter som inlärts med amfetamin (tillståndsberoende inlärning). Detta inre tillstånd fungerar som ett diskriminerande stimulus. Neurofarmakologiska studier visar att det amfetamininducerade tillståndet förmedlas av det dopaminerga neurotransmittorsystemet på mesolimbisk nivå. Viktigt är att de diskriminerande egenskaperna hos amfetamin inte har förknippats med dess psykostimulerande effekter14.
Positiva förstärkande effekter
Tekniken med intracerebral självstimulering har använts för att bedöma de ”belönande” effekterna av amfetamin. Detta bygger på att elektrisk stimulering av vissa hjärnområden ger en behaglig känsla. En gemensam egenskap hos missbruksdroger är att de underlättar elektrisk stimulering av dessa centra på grund av sina euforiska egenskaper. Amfetamin ger en ökning av intrakraniell självstimulering och en minskning av den strömtröskel som krävs för att upprätthålla detta beteende15. Den neurokemiska mekanism som är inblandad i denna effekt verkar vara en interaktion mellan den centrala frisättningen av dopamin och noradrenalin16. Å andra sidan bygger många av de studier som bedömer drogers beroendeframkallande potential på en uppskattning av deras förstärkande egenskaper, eftersom dessa är de viktigaste orsakerna till tvångsmässigt narkotikasökande och missbruk. Den förstärkande potentialen hos ett läkemedel, som bestäms av paradigmet med intravenös självadministrering av läkemedel hos djur, är således den tydligaste indikatorn på dess beroendeframkallande potential hos människor. I detta avseende har amfetamin visat sig framkalla självadministrationsbeteende hos råttor17 och apor18 . Amfetamin verkar utöva sina förstärkande egenskaper genom sin verkan på mesolimbiska dopaminerga neuroner. Perifer administrering av amfetamin ökar de extracellulära dopaminnivåerna i nucleus accumbens hos råttor2 och förstörelse av dopaminerga terminaler i nucleus accumbens blockerar självadministrering av amfetamin. Flera studier har visat att behandling med amfetamin som leder till sensibilisering av mesolimbiska dopaminerga neuroner ökar sökandet efter psykostimulerande medel och självadministrerande beteende19 . Stimulering av GABAB-receptorer (gamma-aminosmörsyra B) genom perifer administrering av baclofen har också visat sig minska självadministrering av amfetamin och extracellulära dopaminkoncentrationer i nucleus accumbens hos råttan20.
Effekter hos människor
Subjektiva effekter
Administrering av de viktigaste amfetaminerna hos människor ger stimulerande effekter, med känslor av välbefinnande, eufori, energi, minskad trötthet och sömn, känslor av vakenhet, förbättrad intellektuell och psykomotorisk prestation och minskad hunger. Effekterna börjar en timme efter administrering, är maximala inom 1-3 timmar och kan kvarstå i upp till 8-12 timmar21. När de behagliga effekterna avtar kan det uppstå en känsla av ”krasch”, med dysfori, trötthet, nedstämdhet, depression, irritabilitet, sömnlöshet eller sömnighet. Dessa krascher är mer intensiva om amfetaminanvändningen har varit hög eller upprepad. De konsumeras ofta tvångsmässigt (binge) under en eller två dagar och lämnar individen i ett tillstånd av fysisk och psykisk utmattning (comedown). Det kan ta flera dagar för individen att återhämta sig tills ett nytt sug börjar.
Farmakokinetik
Ampetamin absorberas snabbt efter oralt intag. De högsta plasmanivåerna uppträder inom 1 till 3 timmar, beroende på fysisk aktivitet och mängden mat i magen. Fullständig absorption sker vanligtvis 4 till 6 timmar efter intag. Amfetamin koncentreras i njurarna, lungorna, cerebrospinalvätskan och hjärnan. De är mycket lipofila ämnen som lätt passerar blod-hjärnbarriären. Den normala distributionsvolymen är 5 l/kg kroppsvikt. Under normala förhållanden utsöndras cirka 30 % av amfetaminet i urinen utan att metaboliseras. Denna utsöndring varierar dock beroende på urinens pH-värde. Om pH-värdet i urinen är surt (pH 5,5-6,0) sker elimineringen huvudsakligen genom urinutsöndring och nästan 60 % av den utsöndrade dosen förändras inte av njurarna. Om pH är alkaliskt (pH 7,5-8,0) sker elimineringen huvudsakligen genom deaminering och mindre än 7 % utsöndras oförändrat. Halveringstiden varierar mellan 16 och 31 timmar. Den huvudsakliga metaboliska vägen för amfetamin omfattar dess deaminering av cytokrom P450 för att bilda para-hydroxyamfetamin och fenylaceton. Den senare föreningen oxideras till bensoesyra och utsöndras konjugerad med glukuronsyra eller glycin. Små mängder amfetamin omvandlas till noradrenalin genom oxidation. Hydroxylering producerar en aktiv metabolit, O-hydroxynorepinefrin, som fungerar som en pseudotransmittor och kan förmedla vissa effekter av läkemedlet, särskilt hos kroniska användare.
Läkemedelsinteraktioner
Acetazolamid: kan öka plasmakoncentrationerna av amfetamin.
Alkohol: kan öka plasmakoncentrationerna av amfetamin.
Askorbinsyra: genom att sänka pH i urinen kan öka utsöndringen av amfetamin.
Furazolidon: amfetamin kan framkalla ett hypertensivt svar hos patienter som behandlas med furazolidon.
Guanetidin: amfetamin hämmar det antihypertensiva svaret från guanetidin.
Haloperidol: Det finns begränsade bevis för att haloperidol kan hämma effekterna av amfetamin. Den kliniska betydelsen av denna interaktion är dock inte väl etablerad.
Litiumkarbonat: Det finns vissa isolerade bevis för att denna substans kan hämma effekterna av amfetamin.
Monoaminooxidas (MAO): amfetamin orsakar en hypertensiv reaktion hos patienter som behandlas med MAO-hämmare.
Noradrenalin: amfetaminmissbruk kan öka den vasokonstriktoriska reaktionen av noradrenalin.
Fenotiaziner: amfetamin kan hämma den antipsykotiska effekten av dessa substanser och fenotiaziner kan hämma den anorektiska effekten av amfetamin.
Natriumbikarbonat: höga doser av denna substans hämmar elimineringen av amfetamin och ökar därmed dess effekter.
Tobaksbruk: amfetamin verkar inducera en dosberoende ökning av tobaksbruk.
Tricykliska antidepressiva medel: ökar teoretiskt sett effekten av amfetamin. Det finns dock inga kliniska bevis för detta.
Nedsatta effekter hos människor
Oönskade effekter är delvis en följd av farmakologiska effekter. Dessa kan inträffa när som helst, så att doser som tolereras väl en dag kanske inte tolereras en annan dag, vilket leder till oönskade effekter. Det bör noteras att många användare tar flera piller tillsammans med andra substanser på samma kväll. Det är ibland svårt att fastställa orsaken till toxicitet. I princip kan oönskade effekter observeras på två nivåer:
1. De kan orsaka högt blodtryck, takykardi, allvarliga arytmier, ischemi i hjärtmuskeln (angina) och akut hjärtinfarkt. De är förknippade med en ökad förekomst av pulmonell hypertension. Huvudvärk, skakningar, muskel- och käkspänningar, svindel, ataxi, dystoni, kramper och koma kan förekomma. Svår toxisk hepatit med levernekros, som kan kräva levertransplantation, har rapporterats. Matsmältningseffekter inkluderar illamående och kräkningar, paralytisk ileus och tarmischemi. Livshotande effekter inkluderar subarachnoidalblödning, intrakraniell blödning, hjärninfarkt och trombos i cerebrala venösa sinus.
2. Psykologiskt. Dysphori, sömnlöshet, irritabilitet, agitation, fientlighet och förvirring kan förekomma. Amfetamin ger ofta upphov till aggressivitet och leder till våld och riskbeteende. Psykiatriska störningar inkluderar ångest, ångestattacker, paranoida vanföreställningar eller referensvideor och hallucinationer.
Terapeutisk användning
De nuvarande terapeutiska indikationerna för amfetamin är mycket begränsade.
De rekommenderas inte för att minska hunger vid behandling av fetma. De enda två indikationerna för deras användning är behandling av narkolepsi och uppmärksamhetsstörning hos barn. Hos dessa barn är den vanligaste substansen metylfenidat.
Tack
Forskningsarbetet har finansierats av inrikesministeriet genom den nationella narkotikaplanen, av Carlos III Health Institute (FIS 070709) och av nätverket för beroendesjukdomar RD 06/001/001/001.
Författaren förklarar att det inte föreligger någon intressekonflikt.
Författaren förklarar att det inte föreligger någon intressekonflikt.