Alfenta
Generický název: Alfentanil-hydrochlorid
Dávkovací forma: injekce
Medicínské hodnocení: Drugs.com. Naposledy aktualizováno 22. ledna 2021.
- Nežádoucí účinky
- Dávkování
- Odborné
- Interakce
- Těhotenství
- Další
.
CII
Pouze na lékařský předpis
- Alfenta Popis
- Alfenta – klinická farmakologie
- Indikace a použití přípravku Alfenta
- Kontraindikace
- Upozornění
- Předběžná opatření
- Všeobecně
- Poranění hlavy
- Porucha dýchání
- Poslabená funkce jater nebo ledvin
- Lékové interakce
- Karcinogeneze, mutageneze a poškození fertility
- Těhotenská kategorie C
- Porod a porod
- Kojící matky
- Pediatrické použití
- Nežádoucí účinky
- Výskyt vyšší než 1% – pravděpodobně související s příčinou (odvozeno z klinických studií)
- Výskyt méně než 1 % – pravděpodobně příčinná souvislost (odvozeno z klinických studií)
- Zneužívání drog a drogová závislost
- Předávkování
- Dávkování a způsob podání přípravku Alfenta
- Použití u dětí
- Premedikace
- Neuromuskulární blokátory
- BEZPEČNOST A ZACHÁZENÍ S PŘÍPRAVKEM
- Jak se přípravek Alfenta dodává
Alfenta Popis
Alfenta (Alfentanil hydrochlorid) Injection je opioidní analgetikum s chemickým označením N–4-(methoxymethyl)-4-piperidinyl]-N-fenylpropanamid monohydrochlorid (1:1) s molekulovou hmotností 452.98 a rozdělovacím koeficientem n-oktanol:voda 128:1 při pH 7,4. Strukturní vzorec přípravku Alfenta je:
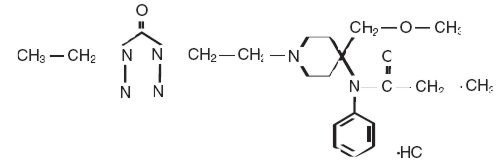
Alfenta je sterilní, nepyrogenní vodný roztok bez konzervačních látek obsahující alfentanil-hydrochlorid odpovídající 500 µg na ml alfentanilové báze pro intravenózní injekci. Roztok, který obsahuje chlorid sodný pro izotonicitu, má pH v rozmezí 4-6. Každý ml obsahuje: Účinná látka: Alfentanil báze 500 mcg. Neúčinné látky:
Alfenta – klinická farmakologie
Alfenta (alfentanil-hydrochlorid) je opioidní analgetikum s rychlým nástupem účinku.
Při dávkách 8-40 mcg/kg u chirurgických zákroků trvajících do 30 minut poskytuje přípravek Alfenta analgetickou ochranu před hemodynamickými reakcemi na chirurgickou zátěž s dobou zotavení obecně srovnatelnou s dobou zotavení pozorovanou u ekvipotentních dávek fentanylu.
Při delších zákrocích tlumí dávky až 75 mcg/kg hemodynamické reakce na laryngoskopii, intubaci a incizi, přičemž doba zotavení je srovnatelná s fentanylem. Při dávkách 50-75 mcg/kg s následnou kontinuální infuzí 0,5-3 mcg/kg/min tlumí přípravek Alfenta katecholaminovou odpověď s rychlejším zotavením a nižší potřebou pooperačních analgetik ve srovnání s pacienty, kterým byl podán enfluran. V dávkách 5 mcg/kg poskytuje přípravek Alfenta analgezii pacientům při vědomí, ale pod sedativy. Na základě reakce pacienta mohou být potřebné dávky vyšší než 5 mcg/kg. Starší nebo oslabení pacienti mohou vyžadovat nižší dávky. Byla zaznamenána vysoká intrasubjektová a intersubjektová variabilita farmakokinetické dispozice přípravku Alfenta.
Farmakokinetiku přípravku Alfenta lze popsat jako tříkompartmentový model se sekvenčními distribučními poločasy 1 a 14 minut; a terminálním eliminačním poločasem 90-111 minut (ve srovnání s terminálním eliminačním poločasem přibližně 475 minut pro fentanyl a přibližně 265 minut pro sufentanil při dávkách 250 mcg). Hlavním místem biotransformace jsou játra.
Alfenta má zdánlivý distribuční objem 0,4-1 l/kg, což je přibližně jedna čtvrtina až jedna desetina distribučního objemu fentanylu, s průměrnou plazmatickou clearance 5 ml/kg/min ve srovnání s přibližně 8 ml/kg/min u fentanylu.
Pouze 1,0 % dávky se vylučuje v nezměněné formě; hlavní cestou eliminace metabolitů je vylučování močí. Vazba přípravku Alfenta na plazmatické bílkoviny je přibližně 92 %.
V jedné studii zahrnující 15 pacientů, kterým byl podáván přípravek Alfenta s oxidem dusným/kyslíkem, bylo prokázáno, že úzké rozmezí plazmatických koncentrací přípravku Alfenta, přibližně 310-340 ng/ml, poskytuje dostatečnou anestezii pro intraabdominální operace, zatímco nižší koncentrace, přibližně 190 ng/ml, blokují reakce na uzavření kůže. Plazmatické koncentrace mezi 100-200 ng/ml poskytovaly adekvátní anestezii pro povrchové operace.
Alfenta má okamžitý nástup účinku. Při dávkách přibližně 105 mcg/kg vyvolává přípravek Alfenta hypnózu stanovenou podle vzorců EEG; na základě schopnosti blokovat reakce na zavedení nazofaryngeálních dýchacích cest byla pro přípravek Alfenta stanovena anestetická ED90 182 mcg/kg u pacientů bez medikace. Na základě klinických studií se požadavky na indukční dávku pohybují v rozmezí 130-245 mcg/kg. U zákroků trvajících 30-60 minut vyvolávají zaváděcí dávky do 50 mcg/kg hemodynamickou odezvu na endotracheální intubaci a kožní incizi srovnatelnou s odezvou na fentanyl. Zaváděcí dávka před intubací 50-75 mcg/kg před kontinuální infuzí tlumí odpověď na laryngoskopii, intubaci a incizi. Následné podání infuze přípravku Alfenta podávané rychlostí 0,5-3 mcg/kg/min s oxidem dusným/kyslíkem tlumí sympatické reakce na chirurgický stres s rychlejším zotavením než enfluran.
Potřeba těkavých inhalačních anestetik se u pacientů, kterým byly podávány anestetické dávky (nad 130 mcg/kg) přípravku Alfenta, snížila během prvních 60 minut udržovací léčby o třicet až padesát procent ve srovnání s pacienty, kterým byly pro úvod do anestezie podávány dávky 4-5 mg/kg thiopentalu. Při anestetických indukčních dávkách přípravek Alfenta poskytuje hlubokou úroveň anestezie během první hodiny udržování anestezie a zajišťuje útlum hemodynamické odpovědi během intubace a incize.
Po anestetické indukční dávce přípravku Alfenta se požadavky na infuzi přípravku Alfenta snižují o 30 až 50 % během první hodiny udržování.
U pacientů se zhoršenou funkcí jater a u pacientů starších 65 let byla zjištěna snížená plazmatická clearance a prodloužená terminální eliminace přípravku Alfenta, což může prodloužit pooperační zotavení. Opakované nebo kontinuální podávání přípravku Alfenta vede ke zvyšování plazmatických koncentrací a ke kumulaci léčiva, zejména u pacientů se sníženou plazmatickou clearance.
U pacientů, kterým je podáván přípravek Alfenta, se může vyskytnout bradykardie. Výskyt a stupeň bradykardie může být výraznější, pokud je přípravek Alfenta podáván společně s nevagolytickými nervosvalovými blokátory nebo v nepřítomnosti anticholinergních látek, jako je atropin.
Bylo prokázáno, že podání intravenózního diazepamu bezprostředně před podáním vysokých dávek přípravku Alfenta nebo po něm vede k poklesu krevního tlaku, který může být sekundární v důsledku vazodilatace; zotavení může být také prodlouženo.
U pacientů, kterým byly podávány dávky do 200 mcg/kg přípravku Alfenta, nebylo zjištěno významné zvýšení hladin histaminu ani klinické známky uvolňování histaminu.
Ztuhlost kosterního svalstva souvisí s dávkou a rychlostí podání přípravku Alfenta. Svalová rigidita se objeví s okamžitým nástupem po indukčních dávkách anestetika. Preventivní opatření (viz UPOZORNĚNÍ) mohou snížit rychlost a závažnost.
Trvání a stupeň respirační deprese a zvýšená rezistence dýchacích cest se obvykle zvyšují s dávkou, ale byly pozorovány i při nižších dávkách. Ačkoli vyšší dávky mohou vyvolat apnoe a delší trvání respirační deprese, apnoe se může objevit i při nízkých dávkách.
Během monitorované anesteziologické péče (MAC) je třeba věnovat pozornost respiračním účinkům přípravku Alfenta Injection. Může dojít ke snížení saturace kyslíkem, apnoe, snížení dechové frekvence a obstrukci horních cest dýchacích. (Viz VAROVÁNÍ)
Indikace a použití přípravku Alfenta
Přípravek Alfenta (alfentanil-hydrochlorid) je indikován:
jako analgetický doplněk podávaný v postupných dávkách při udržování anestezie barbiturátem/oxidem dusným/kyslíkem. jako analgetikum podávané v kontinuální infuzi s oxidem dusným/kyslíkem při udržování celkové anestezie. jako primární anestetikum pro úvod do anestezie u pacientů podstupujících celkovou operaci, u nichž je nutná endotracheální intubace a mechanická ventilace. jako analgetická složka pro monitorovanou anesteziologickou péči (MAC).
VÍCE ÚPLNÝCH INFORMACÍ O POUŽITÍ PŘÍPRAVKU Alfenta naleznete v dávkovací tabulce.
Kontraindikace
Přípravek Alfenta (alfentanil-hydrochlorid) je kontraindikován u pacientů se známou přecitlivělostí na léčivou látku nebo známou nesnášenlivostí jiných opioidních agonistů.
Upozornění
Přípravek Alfenta MUSÍ PODÁVAT POUZE OSOBY SPECIÁLNĚ ŠKOLENÉ V POUŽÍVÁNÍ INTRAVENÓZNÍCH A CELKOVÝCH ANESTETICKÝCH LÁTEK A V ŘÍZENÍ RESPIRAČNÍCH ÚČINKŮ SILNÝCH OPIOIDŮ.
ANTAGONISTA OPIOIDŮ, RESUSCITAČNÍ A INTUBAČNÍ VYBAVENÍ A KYSLÍK BY MĚLY BÝT SNADNO DOSTUPNÉ.
VZHLEDEM K MOŽNOSTI OPOŽDĚNÉ RESPIRAČNÍ DEPRESE MUSÍ MONITOROVÁNÍ PACIENTA POKRAČOVAT I PO OPERACI.
Alfenta (alfentanil-hydrochlorid) podávaná v počátečních dávkách až 20 mcg/kg může způsobit ztuhlost kosterního svalstva, zejména svalů trupu. Výskyt a závažnost svalové rigidity obvykle závisí na dávce. Podání přípravku Alfenta v indukčních anestetických dávkách (nad 130 mcg/kg) trvale vyvolává svalovou rigiditu s okamžitým nástupem. K nástupu svalové rigidity dochází dříve než u jiných opioidů. Přípravek Alfenta může vyvolat svalovou rigiditu, která zahrnuje všechny kosterní svaly, včetně svalů krku a končetin. Výskyt může být snížen: 1) běžnými metodami podávání nervosvalových blokátorů pro vyváženou opioidní anestezii; 2) podáním až 1/4 plné paralyzující dávky nervosvalového blokátoru těsně před podáním přípravku Alfenta v dávkách do 130 mcg/kg; po ztrátě vědomí by měla být podána plná paralyzující dávka nervosvalového blokátoru; nebo 3) současné podání přípravku Alfenta a plné paralyzující dávky nervosvalového blokátoru při použití přípravku Alfenta v rychle podávaných anestetických dávkách (nad 130 mcg/kg).
Použitý nervosvalový blokátor by měl odpovídat kardiovaskulárnímu stavu pacienta. Mělo by být k dispozici odpovídající zařízení pro pooperační monitorování a ventilaci pacientů, kterým byl podán přípravek Alfenta. Je nezbytné, aby tato zařízení byla plně vybavena pro zvládání všech stupňů respirační deprese.
PACIENTI, KTERÝM JE POSKYTOVÁNA MONITOROVANÁ ANESTEZIOLOGICKÁ PÉČE (MAC), BY MĚLI BÝT NEPŘETRŽITĚ MONITOROVÁNI OSOBAMI, KTERÉ SE NEPODÍLEJÍ NA PROVÁDĚNÍ CHIRURGICKÉHO NEBO DIAGNOSTICKÉHO VÝKONU; DOPLŇOVÁNÍ KYSLÍKU BY MĚLO BÝT OKAMŽITĚ K DISPOZICI A POSKYTOVÁNO TAM, KDE JE TO KLINICKY INDIKOVÁNO; SATURACE KYSLÍKEM BY MĚLA BÝT NEPŘETRŽITĚ MONITOROVÁNA; PACIENT BY MĚL BÝT SLEDOVÁN S OHLEDEM NA ČASNÉ ZNÁMKY HYPOTENZE, APNOE, OBSTRUKCE HORNÍCH CEST DÝCHACÍCH A/NEBO DESATURACE KYSLÍKEM.
Závažná a nepředvídatelná potenciace inhibitorů monoaminooxidázy (MAO) byla hlášena u jiných opioidních analgetik a vzácně u alfentanilu. Proto se při podávání alfentanilu pacientům, kteří během 14 dnů dostávali inhibitory MAO, doporučuje vhodné monitorování a pohotová dostupnost vazodilatancií a beta-blokátorů pro léčbu hypertenze.
Předběžná opatření
Byly také hlášeny opožděná RESPIRAČNÍ DEPRESE, RESPIRAČNÍ ARREST, BRADYKARDIE, ASYSTOLIE, ARRHYTHMIAS A HYPOTENZE. PROTO JE TŘEBA ŽIVOTNÍ ZNAKY KONTROLOVAT KONTINUÁLNĚ.
Všeobecně
U starších a oslabených pacientů je třeba počáteční dávku přípravku Alfenta (alfentanil-hydrochlorid) přiměřeně snížit. Účinek počáteční dávky by měl být zohledněn při stanovení doplňkových dávek. U obézních pacientů (více než 20 % nad ideální celkovou tělesnou hmotností) by měla být dávka přípravku Alfenta stanovena na základě štíhlé tělesné hmotnosti.
V jedné klinické studii byla dávka přípravku Alfenta potřebná k navození anestezie, stanovená podle výskytu delta vln v EEG, u geriatrických pacientů o 40 % nižší než dávka potřebná u zdravých mladých pacientů.
U pacientů s poruchou funkce jater a u geriatrických pacientů může být plazmatická clearance přípravku Alfenta snížena a pooperační zotavení může být prodlouženo.
Indukční dávky přípravku Alfenta by měly být podávány pomalu (během tří minut). Podání může vyvolat ztrátu cévního tonu a hypotenzi. Před indukcí je třeba zvážit náhradu tekutin.
Diazepam podaný bezprostředně před podáním vysokých dávek přípravku Alfenta nebo ve spojení s nimi může vyvolat vazodilataci, hypotenzi a vést k opožděnému zotavení.
Bradykardii vyvolanou přípravkem Alfenta lze léčit atropinem. Těžká bradykardie a asystolie byly úspěšně léčeny atropinem a běžnými resuscitačními metodami.
Při výběru nervosvalového blokátoru je třeba zvážit hemodynamické účinky konkrétního svalového relaxancia a požadovaný stupeň relaxace kosterního svalstva.
Po indukční anestetické dávce přípravku Alfenta se požadavky na těkavá inhalační anestetika nebo infuzi přípravku Alfenta snižují o 30 až 50 % pro první hodinu udržovací anestezie.
Infuze přípravku Alfenta by měla být při celkové anestezii přerušena nejméně 10-15 minut před ukončením operace. Během podávání přípravku Alfenta při monitorované anesteziologické péči (MAC) lze v infuzích pokračovat až do konce zákroku.
Respirační depresi způsobenou opioidními analgetiky lze zvrátit opioidními antagonisty, jako je naloxon. Vzhledem k tomu, že trvání respirační deprese vyvolané přípravkem Alfenta může trvat déle než trvání účinku antagonisty opioidů, je třeba zachovat odpovídající dohled. Stejně jako u všech silných opioidů je hluboká analgezie doprovázena respirační depresí a sníženou citlivostí na stimulaci CO2, která může přetrvávat do pooperačního období nebo se může opakovat. Intraoperační hyperventilace může dále změnit pooperační odpověď na CO2. Před propuštěním pacienta z pooperační zóny by mělo být použito vhodné pooperační monitorování, zejména po infuzích a velkých dávkách přípravku Alfenta, aby bylo zajištěno, že je zavedeno a udržováno přiměřené spontánní dýchání bez stimulace.
Poranění hlavy
Přípravek Alfenta by měl být používán s opatrností u pacientů s poraněním hlavy nebo zvýšeným nitrolebním tlakem, a to z důvodu zvýšeného rizika respirační deprese. Stejně jako u všech opioidů může přípravek Alfenta zastřít klinický průběh u pacientů s poraněním hlavy a měl by být používán pouze v případě klinické indikace.
Porucha dýchání
Přípravek Alfenta by měl být používán s opatrností u pacientů s plicním onemocněním, sníženou dechovou rezervou nebo potenciální poruchou dýchání. U takových pacientů mohou opioidy dodatečně snížit dechovou vzpruhu a zvýšit odpor dýchacích cest. Během anestezie to lze zvládnout asistovaným nebo řízeným dýcháním.
Poslabená funkce jater nebo ledvin
U pacientů s poruchou funkce jater nebo ledvin by měl být přípravek Alfenta podáván s opatrností vzhledem k významu těchto orgánů pro metabolismus a vylučování přípravku Alfenta.
Lékové interakce
Míra a trvání účinků na centrální nervový systém a kardiovaskulární systém se může zvýšit, pokud je přípravek Alfenta podáván v kombinaci s jinými látkami tlumícími CNS, jako jsou barbituráty, trankvilizéry, opioidy nebo inhalační celková anestetika. Pooperační respirační deprese může být těmito látkami zesílena nebo prodloužena. V takových případech kombinované léčby by měla být dávka jedné nebo obou látek snížena. Omezené klinické zkušenosti ukazují, že požadavky na těkavá inhalační anestetika se snižují o 30 až 50 % během prvních šedesáti (60) minut po indukci přípravkem Alfenta.
Současné užívání erytromycinu s přípravkem Alfenta může významně inhibovat clearance přípravku Alfenta a může zvýšit riziko prodloužené nebo opožděné respirační deprese.
Cimetidin snižuje clearance přípravku Alfenta. Proto budou při delším podávání nutné menší dávky přípravku Alfenta a doba působení přípravku Alfenta se může prodloužit.
Perioperační podávání léků ovlivňujících průtok krve játry nebo funkci enzymů může snížit plazmatickou clearance a prodloužit rekonvalescenci.
Karcinogeneze, mutageneze a poškození fertility
Nebyly provedeny žádné dlouhodobé studie přípravku Alfenta na zvířatech, které by hodnotily karcinogenní potenciál. V mikrojádrovém testu in vivo u samic potkanů nedošlo k žádným strukturálním chromozomovým mutacím při jednorázových intravenózních dávkách přípravku Alfenta až 20 mg/kg tělesné hmotnosti (přibližně 40násobek horní dávky pro člověka), což odpovídá dávce 103 mg/m2 tělesného povrchu. V in vivo testu dominantní letality u myších samců a samic při maximální intravenózní dávce 20 mg/kg (60 mg/m2) nedošlo k žádným dominantním letálním mutacím. V Amesově testu in vitro na Salmonella typhimurium s metabolickou aktivací i bez ní nebyla zjištěna žádná mutagenní aktivita.
Těhotenská kategorie C
Bylo prokázáno, že přípravek Alfenta má embryocidní účinek u potkanů a králíků, pokud je podáván v dávkách 2,5krát vyšších než je horní dávka pro člověka po dobu 10 dnů až více než 30 dnů. Tyto účinky mohly být způsobeny toxicitou pro matku (snížená spotřeba potravy se zvýšenou úmrtností) po dlouhodobém podávání přípravku.
Po podání přípravku Alfenta u potkanů nebo králíků nebyly pozorovány žádné důkazy teratogenních účinků.
Neexistují žádné adekvátní a dobře kontrolované studie u těhotných žen. Přípravek Alfenta by měl být během těhotenství používán pouze v případě, že potenciální přínos ospravedlňuje potenciální riziko pro plod.
Porod a porod
Nejsou k dispozici dostatečné údaje podporující použití přípravku Alfenta při porodu. Byl hlášen placentární přenos přípravku, proto se použití při porodu nedoporučuje.
Kojící matky
V jedné studii na devíti ženách podstupujících poporodní podvázání vejcovodů byly zjištěny významné hladiny přípravku Alfenta v kolostru čtyři hodiny po podání 60 mcg/kg přípravku Alfenta, přičemž po 28 hodinách nebyly přítomny žádné detekovatelné hladiny. Při podávání přípravku Alfenta kojícím ženám je třeba dbát zvýšené opatrnosti.
Pediatrické použití
V současné době nejsou k dispozici dostatečné údaje podporující použití přípravku Alfenta u dětí mladších 12 let.
Nežádoucí účinky
Nejčastějšími nežádoucími účinky opioidů jsou respirační deprese a ztuhlost kosterního svalstva, zejména svalstva trupu. Alfenta může vyvolat svalovou rigiditu, která zahrnuje kosterní svaly krku a končetin. Viz KLINICKÁ FARMAKOLOGIE, VAROVÁNÍ a OPATŘENÍ týkající se léčby respirační deprese a rigidity kosterního svalstva.
Profil nežádoucích zkušeností od 696 pacientů, kteří dostávali přípravek Alfenta při monitorované anesteziologické péči (MAC), je podobný profilu zjištěnému u přípravku Alfenta při celkové anestezii. Respirační příhody hlášené během MAC zahrnovaly hypoxii, apnoe a bradypnoe. Dalšími nežádoucími účinky hlášenými pacienty, kteří dostávali přípravek Alfenta pro MAC, byly v pořadí podle klesající frekvence nauzea, hypotenze, zvracení, pruritus, zmatenost, somnolence a agitovanost.
Následující informace o nežádoucích účincích pocházejí z kontrolovaných a otevřených klinických studií u 785 pacientů, kteří dostávali intravenózně přípravek Alfenta během úvodu a udržování celkové anestezie. Kontrolované studie zahrnovaly srovnání léčby s fentanylem, thiopentalem sodným, enfluranem, fyziologickým roztokem placebem a halotanem. Výskyt některých nežádoucích účinků je ovlivněn typem použití, např. rigidita hrudní stěny má vyšší hlášený výskyt v klinických studiích indukce alfentanilem, a typem operace, např. nevolnost a zvracení mají vyšší hlášený výskyt u pacientek podstupujících gynekologickou operaci. Celková hlášení nevolnosti a zvracení u přípravku Alfenta byla srovnatelná s fentanylem.
Výskyt vyšší než 1% – pravděpodobně související s příčinou (odvozeno z klinických studií)
| * Výskyt 3% až 9% Všechny ostatní 1% až 3% |
|
| Gastrointestinální: | nevolnost (28 %), zvracení (18 %) |
| Kardiovaskulární: | arytmie, bradykardie (14%), hypertenze (18%), hypotenze (10%), tachykardie (12%) |
| Muskuloskeletální: | rigidita hrudní stěny (17 %), pohyby kosterního svalstva* |
| Dýchací: | apnoe*, pooperační respirační deprese |
| Centrální nervový systém: | rozmazané vidění, závratě*, ospalost/pooperační sedace |
Výskyt méně než 1 % – pravděpodobně příčinná souvislost (odvozeno z klinických studií)
Nežádoucí účinky hlášené v rámci postmarketingového sledování, které nebyly pozorovány v klinických studiích, jsou vyznačeny kurzívou.
| * Výskyt 0.3 % až 1 % | |
| Tělo jako celek: | anafylaxe |
| Centrální nervový systém: | bolest hlavy*, myoklonické pohyby, pooperační zmatenost*, pooperační euforie*, třes* |
| Dermatologický: | svědění*, kopřivka* |
| Místo vpichu: | bolest* |
| Muskuloskeletální: | ztuhlost kosterního svalstva krku a končetin |
| Dýchací: | bronchospasmus, hyperkarbie*, laryngospasmus* |
Zneužívání drog a drogová závislost
Alfenta (alfentanil-hydrochlorid) je regulovaná léčivá látka zařazená do seznamu II, která může vyvolat drogovou závislost morfinového typu, a proto má potenciál být zneužita.
Opioidní analgetika jsou spojována se zneužíváním a závislostí u zdravotníků a dalších osob, které mají k těmto lékům snadný přístup. S přípravkem Alfenta by se mělo zacházet odpovídajícím způsobem.
Předávkování
Předávkování by se projevilo rozšířením farmakologických účinků přípravku Alfenta (alfentanil-hydrochlorid) (viz KLINICKÁ FARMAKOLOGIE) stejně jako u jiných silných opioidních analgetik. Během klinických studií nebyly hlášeny žádné zkušenosti s předávkováním přípravkem Alfenta. Intravenózní LD50 přípravku Alfenta je 43-51 mg/kg u potkanů, 72-74 mg/kg u myší, 72-82 mg/kg u morčat a 60-88 mg/kg u psů. Jako specifické antidotum pro zvládnutí respirační deprese by mělo být použito intravenózní podání antagonisty opioidů, jako je naloxon.
Trvání respirační deprese po předávkování přípravkem Alfenta může být delší než trvání účinku antagonisty opioidů. Podání opioidního antagonisty by nemělo bránit okamžitému zajištění průchodných dýchacích cest, podání kyslíku a asistované nebo řízené ventilaci podle indikace při hypoventilaci nebo apnoi. Pokud je respirační deprese spojena se svalovou rigiditou, může být k usnadnění asistované nebo řízené ventilace zapotřebí použít nervosvalový blokátor. Ke zvládnutí hemodynamické nestability mohou být zapotřebí intravenózní tekutiny a vazoaktivní látky.
Dávkování a způsob podání přípravku Alfenta
Dávkování přípravku Alfenta (alfentanil-hydrochlorid) by mělo být u každého pacienta individualizováno a titrováno k dosažení požadovaného účinku podle tělesné hmotnosti, fyzického stavu, základního patologického stavu, použití jiných léků a typu a trvání chirurgického výkonu a anestezie. U obézních pacientů (více než 20 % nad ideální celkovou tělesnou hmotností) by měla být dávka přípravku Alfenta stanovena na základě štíhlé tělesné hmotnosti. U starších nebo oslabených pacientů by měla být dávka přípravku Alfenta snížena (viz PRECAUTIONS).
Životní funkce by měly být rutinně monitorovány.
Podle pokynů pro dávkování přípravku Alfenta: 1) přírůstkovou injekcí jako analgetický doplněk k anestezii barbiturátem/kyslíkem dusným/kyslíkem u krátkých chirurgických výkonů (předpokládaná doba trvání kratší než jedna hodina); 2) kontinuální infuzí jako udržovací analgetikum s oxidem dusným/kyslíkem u celkových chirurgických výkonů; a 3) intravenózní injekcí v anestetických dávkách pro úvod do anestezie u celkových chirurgických výkonů s předpokládanou dobou trvání nejméně 45 minut; a 4) intravenózní injekcí jako analgetická složka pro monitorovanou anesteziologickou péči (MAC).
| DÁVKOVÁNÍ BY MĚLO BÝT INDIVIDUALIZOVÁNO A TITROVÁNO | |
|---|---|
| PRO POUŽITÍ. PŘI CELKOVÉ ANESTÉZII | |
| SPONTÁNNÍ DÝCHÁNÍ/ASISTOVANÁ VENTILACE | Indukce analgezie: 8-20 mcg/kg Udržování analgezie: 3-5 mcg/kg q 5-20 min nebo 0.5 až 1 mcg/kg/min Celková dávka: 8-40 mcg/kg |
| ASISTOVANÁ NEBO KONTROLOVANÁ VENTILACE | |
| Inkrementální injekce (K oslabení reakce na laryngoskopii a intubaci) |
Indukce analgezie: 20-50 mcg/kg Udržování analgezie: 5-15 mcg/kg q 5-20 min Celková dávka: Až 75 mcg/kg |
| Kontinuální infuze (K zajištění útlumu reakce na intubaci a incizi) |
Rychlost infuze je různá a měla by být titrována podle požadovaného klinického účinku. Níže jsou uvedeny pokyny pro dávkování infuze. Indukce analgezie: 50-75 mcg/kg Udržování analgezie: 0,5 až 3 mcg/kg/min (průměrná rychlost 1 až 1,5 mcg/kg/min) Celková dávka: V závislosti na délce trvání zákroku |
| Indukce anestezie | Indukce anestezie: 130-245 mcg/kg Udržování anestezie: 0,5 až 1,5 mcg/kg/min nebo celková anestezie Celková dávka: V závislosti na délce trvání zákroku Při těchto dávkách je třeba počítat se ztuhlostí kmene a použít svalový relaxant. Podává se pomalu (během 3 minut). Koncentrace inhalačních látek se na počáteční hodinu snižuje o 30-50 %. |
| MONITOROVANÁ ANESTEZIOLOGICKÁ PÉČE (MAC) (Pro sedované a citlivé, spontánně dýchající pacienty) |
Indukce MAC: 3-8 mcg/kg Udržování MAC: 3-5 mcg/kg q 5-20 min nebo 0.25 až 1 mcg/kg/min Celková dávka: 3-40 mcg/kg |
Kontinuální infuze: 0,5-3 mcg/kg/min podávaná s oxidem dusným/kyslíkem u pacientů podstupujících celkovou operaci. Po indukční anestetické dávce přípravku Alfenta se požadavky na rychlost infuze snižují o 30-50 % pro první hodinu udržovací infuze.
Změny vitálních funkcí, které naznačují reakci na chirurgický stres nebo odlehčení anestezie, lze kontrolovat zvýšením dávky Alfentanilu na maximálně 4 mcg/kg/min a/nebo podáním bolusových dávek 7 mcg/kg. Pokud se změny nepodaří zvládnout po třech bolusových dávkách podaných během pěti minut, je třeba použít barbiturát, vazodilatační a/nebo inhalační látku. Při absenci těchto příznaků by měla být rychlost infuze vždy upravena směrem dolů, dokud nedojde k určité odpovědi na chirurgickou stimulaci.
Spíše než zvýšení rychlosti infuze by měly být v reakci na příznaky zesvětlení anestezie během posledních 15 minut operace podány bolusové dávky 7 mcg/kg přípravku Alfenta nebo silného inhalačního činidla. Infuze přípravku Alfenta by měla být ukončena nejméně 10-15 minut před ukončením operace.
Použití u dětí
Klinické údaje podporující použití přípravku Alfenta u pacientů mladších 12 let nejsou v současné době k dispozici. Proto se takové použití nedoporučuje.
Premedikace
Výběr preanestetik by měl vycházet z potřeb konkrétního pacienta.
Neuromuskulární blokátory
Vybraný neuromuskulární blokátor by měl být kompatibilní se stavem pacienta s ohledem na hemodynamické účinky konkrétního svalového relaxancia a požadovaný stupeň relaxace kosterního svalstva (viz části KLINICKÁ FARMAKOLOGIE, VAROVÁNÍ a OPATŘENÍ).
U pacientů, kterým jsou podávány anestetické (indukční) dávky přípravku Alfenta, je nezbytné, aby byl k dispozici kvalifikovaný personál a odpovídající zařízení pro zvládání intraoperační a pooperační respirační deprese.
Také viz oddíly UPOZORNĚNÍ a PRAVIDLA.
Pro účely přesného podávání malých objemů přípravku Alfenta se doporučuje používat tuberkulinovou stříkačku nebo její ekvivalent.
Fyzikální a chemická kompatibilita přípravku Alfenta byla prokázána v roztoku s fyziologickým roztokem, 5% dextrózou ve fyziologickém roztoku, 5% dextrózou ve vodě a Lactated Ringers. Klinické studie infuze přípravku Alfenta byly provedeny s přípravkem Alfenta zředěným na koncentrační rozmezí 25 mcg/ml až 80 mcg/ml.
Příklad přípravy přípravku Alfenta k infuzi: 20 ml přípravku Alfenta přidaných do 230 ml ředicího roztoku poskytuje 40 mcg/ml roztoku přípravku Alfenta.
Před podáním je třeba přípravek vizuálně zkontrolovat na přítomnost částic a změnu barvy, kdykoli to roztok a obal dovolí.
BEZPEČNOST A ZACHÁZENÍ S PŘÍPRAVKEM
Přípravek Alfenta (alfentanil-hydrochlorid) je dodáván v samostatně uzavřených lékových formách, které nepředstavují žádné známé riziko pro zdravotnické pracovníky, kteří s ním přicházejí do náhodného kontaktu. Náhodná kožní expozice přípravku Alfenta by měla být ošetřena opláchnutím postiženého místa vodou.
Chraňte před světlem. Uchovávejte: Uchovávejte při teplotě 20° až 25°C. .
Jak se přípravek Alfenta dodává
Alfenta (alfentanil-hydrochlorid) injekce pro intravenózní podání. Každý ml obsahuje: Účinnou látku: Alfentanil báze 500 mcg. Neúčinné látky: Alfentenfalentan: 1: Chlorid sodný 9 mg a WFI Q.S Alfenta Injection je dostupná jako:
NDC 11098-060-02, 2 ml ampule v balení po 10
NDC 11098-060-05, 5 ml ampule v balení po 10
NDC 11098-060-10, 10 ml ampule v balení po 5
NDC 11098-060-20, 20 ml ampule v balení po 5
U.S. Patent č. 4,167,574
květen 1995, listopad 1995
TAYLOR PHARMACEUTICALS
AN AKORN COMPANY
Decatur, IL 62522
AFA0N Rev. 06/05
| Alfenta Alfentanil hydrochlorid injekce |
|||||||||||||||||||||||||||||||
|
|||||||||||||||||||||||||||||||
|
|||||||||||||||||||||||||||||||
|
|||||||||||||||||||||||||||||||
|
|||||||||||||||||||||||||||||||
Označovač – TAYLOR PHARMACEUTICALS
.