Amfetaminy | Návykové poruchy
Původ amfetaminu
Amfetamin byl poprvé syntetizován v roce 1887 L. Edelanem. V roce 1920 Gordon Alles zjistil, že výchozí sloučenina, amfetamin sulfát, a její ještě účinnější dextroizomer, dextroamfetamin sulfát, mají schopnost stimulovat centrální nervový systém (CNS). V roce 1931 jej začaly zkoumat farmaceutické laboratoře ve Spojených státech a o pět let později, v době prohibice, jej francouzská farmaceutická společnost Smith Kline &, která získala Allesovy patenty, uvedla do lékařské praxe pod obchodním názvem Benzedrine® (pro štamgasty Bennies). Téměř okamžitě se na trhu objevil jeho účinnější izomer, dextroamfetamin prodávaný pod názvem Dexedrine® (dexies). Po zařazení mezi kontrolované látky se oba typy amfetaminu objevily na americkém černém trhu pod názvy souvisejícími s jejich subjektivními účinky, jako je speed a uppers.
Struktura a klasifikace
Amfetaminy jsou sympatomimetické aminy se strukturním chemickým vzorcem podobným adrenalinu (obr. 1). Dva nejčastěji používané amfetaminy, z nichž jsou odvozeny nejmodernější drogy této skupiny, jsou: d-amfetamin sulfát nebo d-fenyl-isopropylamin (dexedrin), který odpovídá dextrorotátorovému izomeru této látky, a racemický amfetamin sulfát (benzedrin) (obr. 2). Dextrorotační sloučenina (dexedrin nebo d-benzedrin) je dvakrát účinnější než racemická sloučenina (benzedrin) a čtyřikrát účinnější než levorotační sloučenina. Z farmakologického hlediska, když se sloučenina s chemickou strukturou podobnou adrenalinu přesune od adrenalinu k amfetaminům, zvýší se její stimulační aktivita v CNS a sníží se její aktivita v periferní části těla (neurovegetativní systém).
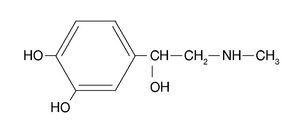
Obrázek 1. Sloučeniny s chemickou strukturou podobnou adrenalinu. Chemická struktura adrenalinu.
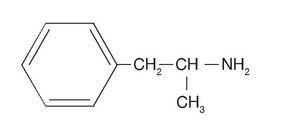
Obrázek 2. Chemická struktura dl-amfetaminu.
Mezi nejčastěji užívané amfetaminové psychostimulační přípravky patří amfetamin, fentermin, chlorfentermin a metamfetamin (obr. 3), přičemž posledně jmenovaný má velký význam, neboť je základem skupiny MDMA (3,4-methylendioxymetamfetamin; extáze). Objevila se také řada sloučenin patřících do neamfetaminové skupiny heterocyklických aminů, které se získávají z kyseliny piperdinoctové, jako je methylfenidát a pripadol. Mezi další heterocyklické aminy patří facetoteran a fenmentracin. Tyto léky jsou relativně nové, ačkoli rostlina, z níž se efedrin získává (Catha edulis), se při léčbě astmatu používala již ve starověku. Od 60. let 20. století se díky reklamě dostalo užívání amfetaminu opět do módy, a to pro jeho chuť k jídlu potlačující (anorektické) vlastnosti.
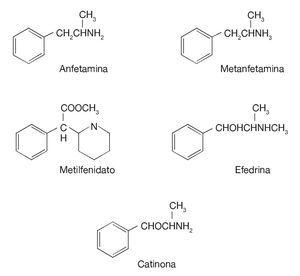
Obrázek 3. Chemická struktura amfetaminu a některých derivátů.
Mechanismy účinku
Amfetaminy mají mechanismus účinku zahrnující několik neurotransmiterů, jako je dopamin, serotonin, adrenalin a noradrenalin.
Zvýšené uvolňování dopaminu
Zvýšená koncentrace neurotransmiteru v synaptickém prostoru vzniká jednak zablokováním zpětného vychytávání, mechanismem podobným jako u kokainu, ale s jiným bodem fixace, jednak zvýšeným uvolňováním, protože d-amfetamin může proniknout do neuronu a vytlačit dopamin z jeho negranulárních cytoplazmatických zásob (obr. 1). 4) s následnou deplecí neurotransmiterů1,2.
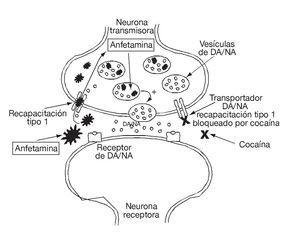
Obrázek 4. Schéma mechanismu účinku amfetaminů na dopaminergní a noradrenergní neurotransmiterový systém. DA: dopamin; NA: noradrenalin.
Toto zvýšení dopaminu v oblastech laterálního hypotalamu v závislosti na dávce reguluje pocit chuti k jídlu. Zatímco zvýšené hladiny dopaminu v nigrostriatálních a mezokortikolimbických drahách (obr. 5) se podílejí na psychostimulačních a odměňujících vlastnostech amfetaminu.
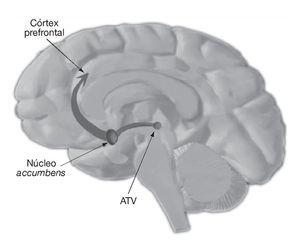
Obrázek 5. VTA: ventrální tegmentální oblast.
Inhibice zpětného vychytávání serotoninu
Amfetamin zvyšuje extracelulární koncentrace serotoninu3 vytěsněním neurotransmiteru z jeho specifického presynaptického transportéru. Když se amfetamin naváže na serotoninové transportéry, jednak zabrání vstupu serotoninu do terminálu, jednak obrátí mechanismus zpětného vychytávání, takže serotonin odchází do synaptického prostoru. Tento mechanismus se zdá být selektivnější pro léky, jako jsou fenfluramin a dexfenfluramin, které rovněž uvolňují serotonin z intracelulárních zásob a jsou schopny aktivovat receptory 5-HT1. Na anorektickém účinku amfetaminů se podílí také zvýšené množství serotoninu.
Zvýšené uvolňování noradrenalinu
Amfetaminy usnadňují uvolňování noradrenalinu tím, že jsou transportovány do nervových zakončení mechanismem zpětného vychytávání (obr. 4). Jakmile se dostanou do nervových zakončení, jsou vychytávány vezikulárním transportérem výměnou za noradrenalin, který uniká do cytosolu. Na adrenergní receptory působí jen slabě. Tento mechanismus by částečně vysvětloval centrální účinky amfetaminů, jako je zvýšená motorická aktivita, snížená únava, a periferní účinky, které tyto drogy provázejí, jako je tachykardie, pocení a potíže s močením.
Přerušení vezikulárního monoaminového transportéru
Vezikulární monoaminový transportér (VMAT2) se nachází především v CNS a je zodpovědný za transport monoaminů přítomných v cytoplazmě do zásobních vezikul. Amfetaminy mohou narušit protonový gradient v membránách těchto synaptických vezikul, a tím i jejich funkci. Obracejí tak tok těchto transportérů, což vede ke zvýšení cytoplazmatických koncentrací noradrenalinu, dopaminu a serotoninu. Protože VMAT2 může hrát roli v lokomotorické stimulaci a posilujících účincích amfetaminů, mohl by být cílem pro vývoj terapeutických strategií pro návykové procesy spojené s užíváním psychostimulancií4.
Farmakologické účinky amfetaminů
Periferně
Amfetaminy vyvolávají periferní vazokonstrikci a v důsledku toho zvýšení systolického i diastolického krevního tlaku. Zvyšuje srdeční frekvenci beta-adrenergním působením, i když ji může také reflexně snižovat. Na úrovni hladkého svalstva stahuje radiální sval duhovky, což vede k mydriáze a zvýšení nitroočního tlaku. Peristaltika je snížena, stejně jako sekrece. Uvolňuje bronchiální svalstvo beta-adrenergním účinkem. Stahuje svěrač močového měchýře, čímž ztěžuje močení.
Na úrovni centrálního nervového systému
Amfetaminy vyvolávají pocit bdělosti, povzbuzení, zlepšení intelektuální výkonnosti a plnění manuálních úkolů, pocit energie, snížení únavy, spánku a hladu. Mají vysoký potenciál zneužívání a mohou vyvolat závislost. U pokusných zvířat amfetaminy způsobují zvýšení lokomotorické aktivity v závislosti na dávce a při vysokých dávkách vyvolávají stereotypie. Předpokládá se, že u lidí může být záchvatovité přejídání projevem stereotypního chování u zvířat.
Tolerance
Po opakovaném užití amfetaminů a jejich derivátů dochází k fenoménu tolerance jak subjektivních, tak objektivních účinků, takže k dosažení stejného účinku je třeba vyšších dávek.
Tato tolerance může být chronická nebo akutní (tachyfylaxe). Navrhovaný mechanismus tolerance nebo desenzibilizace zahrnuje fosforylaci receptoru, která vyvolává rozpojení mezi G proteinem a samotným receptorem5. Chronická i akutní tolerance jsou částečně zodpovědné za tendenci zneužívat deriváty amfetaminu při hledání stimulačních účinků. Tachyfylaxe naopak může vést k život ohrožujícímu předávkování. Klinicky byla pozorována zkřížená tolerance mezi sympatomimetiky amfetaminového typu a u potkanů byla prokázána zkřížená tolerance mezi anorexickým účinkem kokainu a amfetaminu. Kromě toho byla popsána reverzní tolerance nebo senzibilizace, která je charakteristická pro užívání derivátů amfetaminu a projevuje se jako stav předávkování po požití obvyklých dávek.
Senzibilizace
Senzibilizace chování znamená zvýšenou reaktivitu na amfetamin po opakovaném podání. Ventrální tegmentální oblast (VTA) se podílí na indukci amfetaminem zprostředkované senzibilizace chování6. Projev senzibilizace je pravděpodobně způsoben desenzibilizací presynaptických D2 dopaminergních receptorů, které negativně modulují uvolňování dopaminu v některých oblastech mozku, jako je nucleus accumbens. Podání léku tedy povede k dalšímu zvýšení synaptického dopaminu a následnému zvýšení intenzity účinku. Senzibilizace může být dlouhodobá a zdá se, že se rozvíjí rychleji, pokud je lék podáván přerušovaně. Nedávno byl popsán další mechanismus, který se snaží vysvětlit senzibilizaci. Amfetaminy (d-amfetamin a fenfluramin) jsou tedy schopny využít presynaptický transportér pro serotonin jeho vytěsněním, čímž zabrání fosforylaci vedoucí k intracelulární distribuci serotoninu a zvýší počet transportérů dostupných v membráně pro následné dávky léčiva. Tato redistribuce proteinů zpětného vychytávání v membráně může představovat některé z molekulárních změn, které se podílejí na senzibilizaci na stimulační účinky. Předpokládá se, že tento jev je zodpovědný za psychotické stavy, které někdy doprovázejí užívání těchto drog.
Závislost
Amfetaminy se zpočátku užívají v jednorázových dávkách a vyvolávají euforii a posílení (fáze nástupu) především díky své schopnosti uvolňovat dopamin na dopaminergních terminálech v mezokortikolimbické dráze (nucleus accumbens a prefrontální kůra). Se zvyšující se spotřebou (konsolidační fáze) vzniká tolerance, kterou lze překonat zvýšením dávek nebo změnou způsobu podání. V této fázi dochází k vyčerpání dopaminu. Vzniká tolerance a začíná přejídání, aby se euforie udržela. Flám trvá přibližně 12-48 hodin a končí vyčerpáním subjektu, který potřebuje několik dní na zotavení. V této fázi jsou hladiny dopaminu velmi nízké a mohou být přítomny neuronální poruchy.
Pro amfetaminy a syntetické drogy platí obecná kritéria zneužívání (méně časté užívání než závislost) Diagnostického a statistického manuálu duševních poruch IV (DSM-IV). Je u nich pozorována noncompliance, užívání v rizikových situacích a mohou mít kvůli užívání a jeho důsledkům právní, sociální a mezilidské problémy.
Obecná kritéria DSM-IV pro závislost na amfetaminech se vztahují i na amfetaminy. Závislost na amfetaminu je doprovázena intenzivní tolerancí, odvykáním a ústupem od obvyklých činností. Vzniká neodolatelná potřeba užívání (craving). Při užívání se často objevují psychotické příznaky. Náhlé ukončení chronického užívání amfetaminu je charakterizováno nástupem abstinenčního syndromu s různými fázemi. Počáteční fáze (pád) začíná během několika hodin a trvá až 9 dní. Objevuje se dysforie, deprese, anergie, agitovanost, úzkost, nespavost, hypersomnolence, hyperfagie a intenzivní bažení. Střední nebo abstinenční fáze se objevuje mezi 1 a 10 týdny. Zpočátku se projevuje únavou, nedostatkem energie, anhedonií a depresí. Touha se snižuje, a pokud nedojde k recidivě, depresivní příznaky se postupně zlepšují. Ve třetí fázi, která je neurčitá, se mohou objevit intenzivní epizody cravingu, obvykle související s podmíněnými signály, které mohou u pacienta způsobit relaps. U osob, které požily velké dávky, se mohou objevit sebevražedné myšlenky. Podobný obraz byl popsán u kokainu. Neexistuje žádná specifická farmakologická léčba závislosti na amfetaminu. Protože se zdá, že během odvykání může dojít k poklesu dopaminu, používají se agonisté dopaminu a antidepresiva. Výsledky s psychotropními léky jsou neuspokojivé. Nápomocná může být psychoterapie. Poruchy vyvolané amfetaminy se léčí symptomaticky, antipsychotiky při psychotických projevech a anxiolytiky při úzkosti a záchvatech paniky nebo panické poruše. Nedávno byl podán přehled farmakologických účinků metamfetaminu7.
Nurotoxicita metamfetaminu
Nurotoxicita vyvolaná látkou je definována jako škodlivá strukturální nebo funkční změna CNS. Neurotoxicita způsobená amfetaminy tedy obvykle znamená přetrvávající změny na neurochemické a neuronální úrovni, včetně lézí v axonech a zakončeních obsahujících monoaminy. U potkanů a opic způsobuje podávání metamfetaminu pokles dopaminu a jeho metabolitů8. U potkanů metamfetamin rovněž snižuje hladinu serotoninu, místa zpětného vychytávání dopaminu a serotoninu, snižuje aktivitu enzymů podílejících se na syntéze neurotransmiterů (tyrosinhydroxylázy a/nebo tryptofanhydroxylázy) a vyvolává morfologické změny v neuronech9. Strukturální změny neuronů jsou pozorovány v axonech a zahrnují výskyt varixů a zmenšení a ochuzení axonů. Mezi faktory ovlivňující vznik neurotoxicity metamfetaminu patří použité dávky, počet expozic droze, interval mezi jednotlivými dávkami a doba, po kterou jsou neurony vystaveny působení drogy. Ačkoli jsou údaje o lidech velmi omezené, některé studie naznačují, že metamfetamin u lidí může vyvolat přetrvávající dopaminergní neurotoxicitu spojenou s funkčními změnami, ale byla také pozorována určitá regenerace postižených neuronů několik měsíců po ukončení užívání drogy10.
Neurobiologické studie na laboratorních zvířatech
Účinky na pohybovou aktivitu
Amfetaminy vyvolávají centrální stimulaci11 , což je termín používaný pro popis jejich účinků na pohybovou aktivitu u zvířat a na spánek a elektroencefalografickou aktivitu. Zpočátku amfetamin vyvolává stav bdělosti doprovázený nárůstem exploračního chování, groomingu, vertikální a horizontální lokomoce, po němž následuje pokles těchto aktivit ve prospěch stereotypního chování (odpověď na dávku ve tvaru obráceného U). Neuroanatomické studie ukazují, že zvýšení lokomoční aktivity vyvolané amfetaminy je závislé na nigrostriatálním a mezolimbickém dopaminergním systému. Kromě toho může být při hyperlokomoci důležité centrální uvolňování noradrenalinu. Na druhou stranu se zdá, že stereotypie jsou zprostředkovány uvolňováním nově syntetizovaného dopaminu v nigrostriatálních a mezolimbických dopaminergních drahách a jsou regulovány rovnováhou mezi dopaminergním a cholinergním systémem.
Účinky na agresivní chování
Účinky amfetaminu na agresivní chování u zvířat jsou komplexní a závisí na podané dávce a použitém experimentálním paradigmatu. Důležitá je také role environmentálních faktorů a genetických determinant v těchto účincích. U zvířat i lidí mohou amfetaminy vyvolat epizody extrémní agrese a stažení se z jakékoli sociální výměny. Neurobiologické mechanismy, které se podílejí na vícenásobných účincích amfetaminu na agresivní chování, jsou spojeny s mechanismy souvisejícími s jeho psychostimulačními vlastnostmi. Jedním z paradigmat používaných ke studiu vlivu těchto látek na agresivní chování je test vetřelce. Tento test zahrnuje konfrontaci mezi domácím zvířetem a vetřelcem a zkoumá biologicky platné chování, jako je podřízení se, obranné chování, útok a útěk. Bylo tedy prokázáno, že amfetamin zvyšuje obranné a útěkové chování za různých experimentálních podmínek a u různých druhů zvířat, a nezdá se, že by tento účinek byl zprostředkován centrálním dopaminergním systémem. Antagonisté dopaminu však zvrátí zesilující účinky agresivního chování vyvolané akutním podáním nízkých dávek amfetaminu.12
Vliv na učení
Většina studií na zvířatech naznačuje, že amfetamin učení nenarušuje a za určitých podmínek ho může dokonce posilovat. Existují však i údaje o škodlivých účincích13. Je prokázáno, že učení pod amfetaminem je lépe zapamatovatelné, pokud je v den testování podán amfetamin, a nikoli fyziologický roztok. Během vysazování amfetaminu se navíc objevují poruchy chování naučeného pod vlivem amfetaminu. Bylo tedy prokázáno, že vnitřní stav vyvolaný amfetaminem u zvířete ovlivňuje učení úkolů naučených pod amfetaminem (učení závislé na stavu). Tento vnitřní stav slouží jako diskriminační podnět. Neurofarmakologické studie ukazují, že stav vyvolaný amfetaminem je zprostředkován dopaminergním neurotransmiterovým systémem na úrovni mezolimbické dráhy. Důležité je, že diskriminační vlastnosti amfetaminu nebyly spojeny s jeho psychostimulačními účinky14.
Pozitivní posilující účinky
K hodnocení „odměňujících“ účinků amfetaminu byla použita technika intracerebrální autostimulace. Vychází ze skutečnosti, že elektrická stimulace určitých oblastí mozku vyvolává příjemný pocit. Společnou vlastností zneužívaných drog je, že díky svým euforizujícím vlastnostem usnadňují elektrickou stimulaci těchto center. Amfetamin způsobuje zvýšení intrakraniální autostimulace a snížení proudového prahu potřebného k udržení tohoto chování15. Neurochemickým mechanismem, který se na tomto účinku podílí, je zřejmě interakce mezi centrálním uvolňováním dopaminu a noradrenalinu16. Na druhé straně je mnoho studií hodnotících návykový potenciál drog založeno na odhadu jejich posilujících vlastností, protože ty jsou hlavním faktorem, který přispívá k nutkavému vyhledávání a zneužívání drog. Posilující potenciál drogy, jak je určen paradigmatem intravenózního samopodávání drog u zvířat, je tedy nejjasnějším ukazatelem jejího návykového potenciálu u lidí. V tomto ohledu bylo prokázáno, že amfetamin vyvolává u potkanů17 a opic18 samopodání. Zdá se, že amfetamin uplatňuje své posilující vlastnosti prostřednictvím svého působení na mezolimbické dopaminergní neurony. Periferní podávání amfetaminu tak zvyšuje extracelulární hladiny dopaminu v nucleus accumbens potkanů2 a destrukce dopaminergních terminálů v nucleus accumbens blokuje samopodávání amfetaminu. Několik studií ukázalo, že léčba amfetaminem, která vyvolává senzibilizaci mezolimbických dopaminergních neuronů, zvyšuje vyhledávání psychostimulancií a chování při samopodávání19 . Bylo také prokázáno, že stimulace receptorů kyseliny gama-aminomáselné B (GABAB) periferním podáním baklofenu snižuje samopodávání amfetaminu a extracelulární koncentrace dopaminu v nucleus accumbens potkana20.
Účinky u lidí
Subjektivní účinky
Podávání hlavních amfetaminů u lidí vyvolává stimulační účinky s pocity pohody, euforie, energie, snížení únavy a spánku, pocity bdělosti, zlepšení intelektuální a psychomotorické výkonnosti a snížení hladu. Účinky začínají hodinu po podání, dosahují maxima během 1-3 hodin a mohou přetrvávat až 8-12 hodin21. Po odeznění příjemných účinků se může dostavit pocit „zhroucení“ s dysforií, únavou, depresí, skleslostí, podrážděností, nespavostí nebo ospalostí. Tyto pády jsou intenzivnější, pokud bylo užívání amfetaminu vysoké nebo opakované. Často jsou konzumovány nutkavě (binge) po dobu jednoho nebo dvou dnů, což zanechává jedince ve stavu fyzického a duševního vyčerpání (comedown). Může trvat několik dní, než se jedinec zotaví, než začne další flám.
Farmakokinetika
Amfetamin se po perorálním požití rychle vstřebává. Nejvyšší plazmatické hladiny se objevují během 1 až 3 hodin v závislosti na fyzické aktivitě a množství potravy v žaludku. K úplnému vstřebání obvykle dochází 4 až 6 hodin po požití. Amfetaminy se koncentrují v ledvinách, plicích, mozkomíšním moku a mozku. Jsou to vysoce lipofilní látky, které snadno procházejí hematoencefalickou bariérou. Normální distribuční objem je 5 l/kg tělesné hmotnosti. Za normálních podmínek se přibližně 30 % amfetaminu vylučuje močí, aniž by byl metabolizován. Toto vylučování se však liší v závislosti na pH moči. Pokud je pH moči kyselé (pH 5,5-6,0), vylučuje se převážně močí a téměř 60 % vyloučené dávky se v ledvinách nezmění. Pokud je pH alkalické (pH 7,5-8,0), vylučuje se převážně deaminací a méně než 7 % se vylučuje v nezměněné formě. Poločas rozpadu se pohybuje od 16 do 31 hodin. Hlavní metabolická cesta amfetaminu zahrnuje jeho deaminaci cytochromem P450 za vzniku para-hydroxyamfetaminu a fenylacetonu. Tato sloučenina se oxiduje na kyselinu benzoovou a vylučuje se konjugovaná s kyselinou glukuronovou nebo glycinem. Malé množství amfetaminu se oxidací mění na noradrenalin. Hydroxylací vzniká aktivní metabolit, O-hydroxynorepinefrin, který působí jako pseudotransmiter a může zprostředkovat některé účinky drogy, zejména u chronických uživatelů.
Lékové interakce
Acetazolamid: může zvýšit plazmatické koncentrace amfetaminu.
Alkohol: může zvýšit plazmatické koncentrace amfetaminu.
Kyselina askorbová: snížením pH moči může zvýšit vylučování amfetaminu.
Furazolidon: amfetaminy mohou u pacientů léčených furazolidonem vyvolat hypertenzní reakci.
Guanethidin: amfetaminy inhibují antihypertenzní odpověď guanethidinu.
Haloperidol: existují omezené důkazy, že haloperidol může inhibovat účinky amfetaminu. Klinický význam této interakce však není dostatečně prokázán.
Karbonát lithia: existují ojedinělé důkazy, že tato látka může inhibovat účinky amfetaminu.
Monoaminooxidáza (MAO): amfetaminy způsobují hypertenzní reakci u pacientů léčených inhibitory MAO.
Noradrenalin: zneužívání amfetaminů může zvýšit vazokonstrikční reakci noradrenalinu.
Fenothiaziny: amfetamin může inhibovat antipsychotický účinek těchto látek a fenothiaziny mohou inhibovat anorektický účinek amfetaminu.
Bikarbonát sodný: vysoké dávky této látky inhibují eliminaci amfetaminu, a tím zvyšují jeho účinky.
Užívání tabáku: zdá se, že amfetamin vyvolává zvýšení užívání tabáku v závislosti na dávce.
Tricyklická antidepresiva: teoreticky zvyšují účinek amfetaminu. Neexistují však pro to žádné klinické důkazy.
Nežádoucí účinky u lidí
Nežádoucí účinky jsou částečně důsledkem farmakologických účinků. Ty se mohou objevit kdykoli, a to do té míry, že dávky, které jsou jeden den dobře snášeny, nemusí být jiný den snášeny, což vede k nežádoucím účinkům. Je třeba poznamenat, že mnoho uživatelů užívá několik tablet společně s dalšími látkami během jedné noci. Někdy je obtížné rozpoznat příčinu toxicity. Nežádoucí účinky lze pozorovat v zásadě na dvou úrovních:
1. Mohou způsobit vysoký krevní tlak, tachykardii, závažné arytmie, ischemii myokardu (anginu pectoris) a akutní infarkt myokardu. Jsou spojeny se zvýšeným výskytem plicní hypertenze. Mohou se objevit bolesti hlavy, třes, svalové a čelistní napětí, závratě, ataxie, dystonie, křeče a kóma. Byla hlášena těžká toxická hepatitida s jaterní nekrózou, která může vyžadovat transplantaci jater. Trávicí účinky zahrnují nevolnost a zvracení, paralytický ileus a střevní ischemii. Mezi život ohrožující účinky patří subarachnoidální krvácení, intrakraniální krvácení, mozkový infarkt a trombóza mozkové žilní dutiny.
2. Psychologické. Může se objevit dysforie, nespavost, podrážděnost, agitovanost, nepřátelství a zmatenost. U amfetaminů se často objevuje agrese, která vede k násilí a rizikovému chování. Psychiatrické poruchy zahrnují úzkost, záchvaty úzkosti, paranoidní bludy nebo referenční bludy a halucinace.
Terapeutické použití
Současné terapeutické indikace amfetaminů jsou velmi omezené.
Nedoporučují se ke snížení hladu při léčbě obezity. Jediné dvě indikace pro jejich použití jsou léčba narkolepsie a poruchy pozornosti u dětí. U těchto dětí je nejčastěji užívanou látkou methylfenidát.
Poděkování
Výzkumná práce je financována Ministerstvem vnitra prostřednictvím Národního protidrogového plánu, Zdravotním ústavem Carlose III (FIS 070709) a Sítí návykových nemocí RD 06/001/001.
Autor prohlašuje, že není ve střetu zájmů.
Autor prohlašuje, že není ve střetu zájmů.