Chemistry Learner
Fluorid bromitý je toxická interhalogenová sloučenina. Je známý pro své použití jako silné fluorizační činidlo.
- Identifikace trifluoridu bromitého
- Chemický vzorec trifluoridu bromu
- Produkce trifluoridu bromu
- Složení trifluoridu bromitého
- Vlastnosti trifluoridu bromu
- Vzhled
- Vůně
- Hygroskopie
- Molární hmotnost
- Monoizotopová hmotnost
- Hustota
- Teplota tání
- Teplota varu
- Vodivost
- Korózní vlastnosti
- Měrná hmotnost
- Dipólový moment
- Rozpustnost
- Struktura trifluoridu bromitého
- Reakce trifluoridu bromu
- Trifluorid bromitý Použití
- Bromtrifluorid MSDS
- Zdravotní rizika
- První pomoc
- Profil reaktivity
- Požární opatření
- Opatření při náhodném úniku
- Manipulace s bromtrifluoridem
- Skladování bromtrifluoridu
- Osobní ochrana
Identifikace trifluoridu bromitého
Číslo CAS: 7787-71-5
Číslo UN: UN1746
Identifikační číslo sloučeniny PubChem: 24594
Referenční číslo ChemSpider: 20474213
Číslo MDL: MFCD00042533
Číslo ES: 232-132-1
Číslo RTECS: ED2275000
Identifikátor InChI: ED2275000
InChI=1S/BrF3/c2-1(3)4
InChI klíč: InChIKey=FQFKTKUFHWNTBN-UHFFFAOYSA-N
Chemický vzorec trifluoridu bromu
Chemický vzorec této interhalogenové sloučeniny je BrF3.
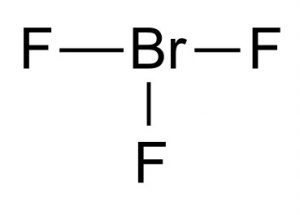
Obrázek 1 – Trifluorid bromu
Produkce trifluoridu bromu
V roce 1906 Paul Lebeau poprvé syntetizoval tuto sloučeninu reakcí bromu s fluorem při teplotě 20 °C. V roce 1906 byla tato sloučenina poprvé syntetizována. Reakci představuje následující rovnice:
Br2 + 3F2 → 2BrF3
Dalším způsobem výroby trifluoridu bromu je současná redukce a oxidace monofluoridu bromu. Při této reakci vzniká trifluorid bromitý a brom.
3BrF → BrF3 + Br2
Složení trifluoridu bromitého
Trifluorid bromitý se skládá z 58,367 % bromu a 41 % bromu.632 % fluoru.
Vlastnosti trifluoridu bromu
Fyzikální a chemické vlastnosti této látky jsou popsány níže:
Vzhled
Je to kapalina slámové barvy.
Vůně
Chemická látka má štiplavý zápach.
Hygroskopie
Jedná se o hygroskopickou kapalinu.
Molární hmotnost
Molární hmotnost trifluoridu bromitého je 136 %.90 g/mol.
Monoizotopová hmotnost
Monoizotopová hmotnost této látky je 135,913547 u (sjednocené jednotky atomové hmotnosti).
Hustota
Hustota této látky je 2,803 g/cm3.
Teplota tání
Teplota tání trifluoridu bromitého je 8,77 °C.
Teplota varu
Teplota varu této látky je 125,72 °C.
Vodivost
Díky autoionizaci je kapalina dobrým vodičem elektrické energie.
Korózní vlastnosti
Jedná se o korozivní kapalinu.
Měrná hmotnost
Měrná hmotnost trifluoridu bromitého je 2,81 při teplotě 68,0 °F.
Dipólový moment
Molekulární dipólový moment této látky je 1,19 Debyeho.
Rozpustnost
Trifluorid bromitý je rozpustný v kyselině sírové. Při styku s organickými sloučeninami a vodou se rozkládá a exploduje. Reakce se sloučeninami obsahujícími vodík mohou způsobit prudké reakce. Mnoho iontových fluoridů se snadno rozpouští v trifluoridu bromu a vytváří solvobáze.
KF + BrF3 → KBrF4
Kromě výše uvedených vlastností je trifluorid bromu také silným fluorizačním činidlem.
Struktura trifluoridu bromitého
Lewisova struktura trifluoridu bromitého ukazuje, že má molekulovou strukturu ve tvaru písmene T. V případě trifluoridu bromitého je jeho molekulová struktura ve tvaru písmene T. V případě trifluoridu bromitého je jeho molekulová struktura ve tvaru písmene T. Podle VSEPR teorie vzniku molekul je centrální brom spojen se dvěma elektronovými páry. Vzdálenost mezi bromovým centrem a ekvatoriálním fluorem je 1,72 Å a ke každému z axiálních fluorů je 1,81 Å. Úhel mezi ekvatoriálním fluorem a axiálním fluorem je 86,2°. Úhel je udržován o něco menší než 90°, protože síla odpuzování z vazeb Br-F je menší než síla elektronových párů.
Reakce trifluoridu bromu
Trifluorid bromu při reakci s oxidy kovů uvolňuje kyslík. Při reakci trifluoridu bromitého s oxidem křemičitým vzniká plynný tetrafluorid křemičitý a brom.
Při reakci trifluoridu bromitého s oxidem titaničitým(IV) vzniká fluorid titaničitý(IV) a brom.
Trifluorid bromitý Použití
Trifluorid bromitý je silné ionizující anorganické rozpouštědlo a fluorizační činidlo. Používá se také k výrobě hexafluoridu uranu (UF6) při zpracování a přepracování jaderného paliva.
Bromtrifluorid MSDS
Zdravotní rizika
Člověk vystavený působení bromtrifluoridu může mít následující zdravotní problémy:
Kontakt s pokožkou: Styk kůže s touto chemickou látkou může vést k pálení a podráždění.
Styk s očima: Pokud se oči dostanou do kontaktu s výpary chemikálie nebo s chemikálií samotnou, může to vést k silnému pálení očí, vředům a dokonce k oslepnutí.
Zažívání:
Při požití dochází k těžkému pálení sliznic: Vdechnutí může vést k těžkému podráždění horních cest dýchacích.
První pomoc
Oči: Oči je třeba důkladně vymývat velkým množstvím vody po dobu nejméně 15 minut. Okamžitě je třeba vyhledat lékaře.
Kůže: Pokud se kůže dostane do kontaktu s chemickou látkou, je třeba zasažená místa dobře omývat vodou a mýdlem po dobu nejméně 15 minut. Je nutná okamžitá lékařská pomoc. Kontaminovaný oděv je třeba rychle odstranit. Před opětovným použitím je třeba oděv důkladně vyčistit a vysušit. Kontaminovaná obuv by měla být zničena.
Potrava: V případě náhodného požití by měl postižený vypít velké množství vody. Vyvolávání zvracení se nedoporučuje.
Vdechnutí: V případě jakýchkoli nežádoucích účinků by měla být oběť odvedena na nekontaminované místo. V případě, že oběť nedýchá, je třeba použít umělé dýchání. Pokud je dýchání a dýchání stále obtížné, měl by být podán kyslík. K zajištění bezpečnosti oběti je nutná další lékařská pomoc.
Profil reaktivity
Trifluorid bromitý je vysoce reaktivní oxidační činidlo. Při styku s vodou reaguje prudce. Může urychlit hoření hořlavé látky. Při styku s látkami obsahujícími vodík, jako je kyselina octová, amoniak a metan, může způsobit výbuch a požár. Při pokojové teplotě také prudce reaguje s kyselinami, halogeny, halogenidy kovů, kovy a oxidy kovů. Konkrétně způsobuje nebezpečné reakce s kyselinou dusičnou, kyselinou sírovou, jódem a selenem.
Požární opatření
Trifluorid bromu je oxidační činidlo, a proto se může při styku s hořlavinami vznítit nebo explodovat.
V případě rozsáhlých požárů by měl být prostor izolován a z bezpečné vzdálenosti zaplaven vodou. Pokud jsou nádoby uchovávající bromtrifluorid v blízkosti požáru, měly by být odstraněny, pokud je to možné bezpečně provést. Nádoby by měly být ochlazovány tekoucí vodou i dlouho po uhašení požáru.
Hasicí prostředky: Při hašení požáru je třeba použít vhodná hasicí média. Pro hašení požáru se doporučuje použití vody, suché chemikálie nebo uhličitanu sodného.
Opatření při náhodném úniku
Hořlavé materiály je třeba izolovat a zabránit jakémukoli spojení s nimi. Rozlitého materiálu by se nemělo sahat. Únik chemické látky by měl být zastaven, pokud je to možné bez osobního rizika. Výskyt chemických výparů by měl být snížen postřikem vodou. Je třeba dbát na to, aby se voda nedostala dovnitř nádob s chemikáliemi. V případě velkých úniků by měly být chemické látky umístěny do karantény, aby mohly být později zlikvidovány. Prostor by měl být řádně větrán.
Manipulace s bromtrifluoridem
Manipulace s tímto materiálem podléhá manipulačním předpisům podle U.S. OSHA 29 CFR 1910.119.
Skladování bromtrifluoridu
Chemická látka by měla být skladována a mělo by se s ní manipulovat podle platných norem a předpisů NFPA 430 Code for the storage of Liquid and Solid Oxidizing Materials. Nádoby s chemikálií by měly být chráněny před jakýmkoli fyzickým poškozením. Měly by být také uchovávány odděleně od jakýchkoli neslučitelných látek.
Osobní ochrana
Při manipulaci s touto chemickou látkou je třeba dbát na odpovídající ochranu. Měly by se používat vhodné ochranné pomůcky. Ty by měly v ideálním případě zahrnovat:
- Pro správné dýchání je nutný autonomní dýchací přístroj podle norem MSHA/NIOSH (schválený nebo ekvivalentní) s kyslíkovou maskou s tlakovou potřebou.
- Pro ochranu očí jsou nutné ochranné brýle nebo ochranné brýle schválené úřadem OSHA.
- K ochraně kůže před škodlivými infekcemi v důsledku kontaktu s chemikáliemi je třeba používat ochranný oděv a rukavice.
Kromě výše uvedených ochranných pomůcek by měl být prostor také dobře větrán. Ventilační mechanismus by měl být odolný proti výbuchu v případě, že jsou přítomny výbušné koncentrace chemické látky. Měl by být rovněž zajištěn místní odsávací systém.