Podívejte se na nejnovější články
27letá žena s anamnézou aterosklerotického kardiovaskulárního onemocnění a vzdáleným infarktem myokardu, astmatem a provokovanou hlubokou žilní trombózou (ukončená antikoagulace) se dostavila se stížnostmi na dva dny se zhoršující bolest na hrudi a dušnost. Popírala horečku, zimnici, produktivní kašel nebo nemocné kontakty. Přiznala 70kilový neúmyslný úbytek hmotnosti během 7 měsíců, sníženou chuť k jídlu, noční pocení, průjem a bušení srdce.
Vitální příznaky ukazovaly srdeční frekvenci 95, krevní tlak 113/74 mmHg, dechovou frekvenci 14, SpO2 95 % na pokojovém vzduchu. Komplexní metabolický panel a kompletní krevní obraz byly v normě. EKG ukázalo normální sinusový rytmus s hypertrofií levé komory a bez ST změn. Vyšetření moči na přítomnost drog bylo pozitivní pouze na kanabinoidy. Kardiální markery byly negativní. Hodnota TSH byla 0,01 mclU/ml (0,31-5,00 mclU/ml).
Hospitalizace 1. den: Rentgenový snímek hrudníku ukázal malou hustotu vystupující nad pravou horní plíci na rozhraní předního 3. a zadního 6. žebra. Následné CT vyšetření plic ukázalo neurčitý homogenní solidní útvar v předním horním mediastinu podél aortálního oblouku o rozměrech přibližně 5,5 cm x 5,3 cm x 2,4 cm v kraniokaudálním, transverzálním a AP rozměru. Masa nebyla kontinuální se štítnou žlázou a nevykazovala cystické ani kalcifikované komponenty . Na CT vyšetření byla zaznamenána tyreomegalie bez ložiskové léze. Srdce bylo normální velikosti bez perikardiálního výpotku a kolabující dolní duté žíly . USG štítné žlázy odhalilo oboustrannou tyromegalii s hypervaskularitou a bez diskrétních uzlů.
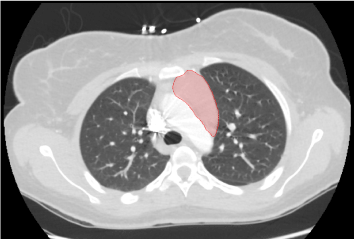
Obrázek 1. Středně velká homogenní solidní masa v horním mediastinu o rozměrech 5,5 cm x 5,3 cm x 2,4 cm.
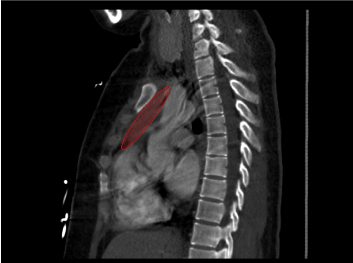
Obrázek 2. Zobrazení hmoty v sagitálním pohledu.
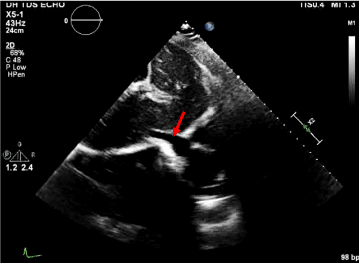
Obrázek 3. Kolabující IVC bez známek perikardiálního výpotku.
Hospitalizační den 2: Vzhledem k podezření na možný lymfom nebo thymom byla konzultována intervenční radiologie a onkologie za účelem získání biopsie přední mediastinální masy k dalšímu zhodnocení .
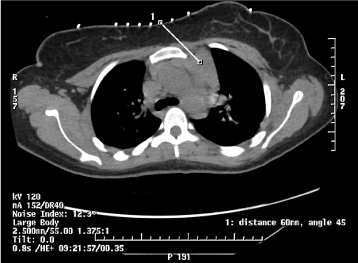
Obrázek 4. CT navigovaná 18-ti jehlová biopsie k získání abnormální hustoty měkkých tkání v přední části levého horního mediastina.
Krátce po návratu z CT navigované jehlové biopsie mediastinální masy se u pacienta objevila nevolnost, profuzní zvracení a přestal reagovat. Po příjezdu týmu rychlé reakce byly vitální funkce následující: srdeční frekvence 150, krevní tlak 65/50 mmHg, RR 20, SpO2 95 % na 6 l kyslíku. EKG ukázalo sinusovou tachykardii bez změn ST. Pacientovi byl podán bolus 1 l fyziologického roztoku a vzhledem k obavě z poranění plicní tepny jako komplikace biopsie byly urgentně připraveny balené červené krvinky. Ultrazvuk u lůžka pacienta odhalil perikardiální výpotek, nekolabující dolní dutou žílu a vzájemnou komorovou závislost prokazující fyziologii tamponády . Pacient byl intubován k ochraně dýchacích cest a byla urgentně konzultována kardiotorakální chirurgie k provedení perikardiocentézy a evakuaci suspektního mediastinálního hematomu. Rentgenový snímek hrudníku potvrdil významné rozšíření mediastina suspektní z mediastinálního hematomu .
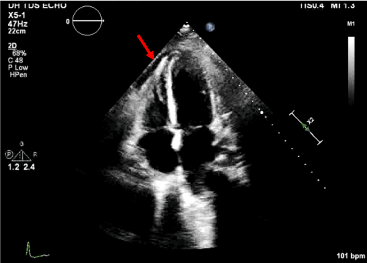
Obrázek 5. Axiální čtyřkomorový snímek s perikardiálním výpotkem.
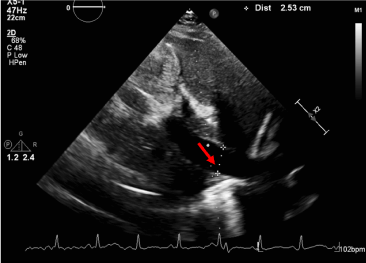
Obrázek 6. Nekolabující dolní dutá žíla. Přítomnost dilatované IVC s méně než 50% kolapsem při forsírovaném vdechu koreluje se zvýšeným centrálním žilním tlakem a potvrzuje fyziologii tamponády.
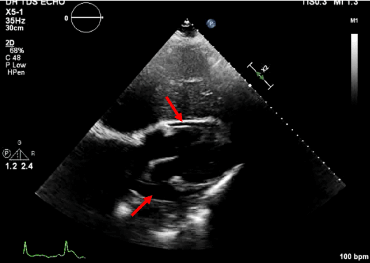
Obr. 7. Přítomnost dilatované IVC s méně než 50% kolapsem při forsírovaném vdechu. Subkostální pohled s perikardiálním výpotkem.
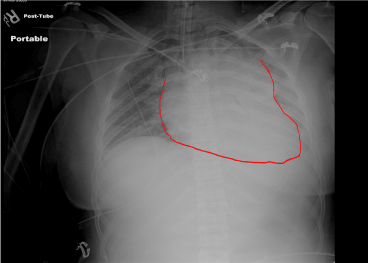
Obrázek 8. Rentgenový snímek po intubaci. Endotracheální rourka v poloze. Rozšířené mediastinum suspektní z mediastinálního hematomu.
Přehled laboratorních vyšetření po převozu pacienta na jednotku intenzivní péče ukázal TSH 0,01 mclU/ml (0,31-5,00 mclU/ml) s reflexním volným T4 > 4,2 ng/dl (0,7-1,7 ng/dl) a T3 > 651 (71-170ng/dl). Protilátka vázající acetylcholinový receptor byla negativní. Burch-Wartofského skóre > 45, což pacienta klasifikovalo jako pacienta s bouří štítné žlázy.
Byla provedena explorativní střední sternotomie s intraoperačním podáním propylthiouracilu, hydrokortizonu sukcinátu sodného a roztoku lugol jodu. Mediastinální explorace odhalila velkou přední mediastinální masu s krvácením, která byla odstraněna. Byly zaznamenány známky penetrace perikardiální stěny; 150 cm3 krve a sraženiny bylo evakuováno. Do každé pleurální dutiny byly zavedeny přímé hrudní trubice. Pacient byl ve stabilizovaném stavu přeložen zpět na jednotku intenzivní péče.
Patologické vyšetření přední mediastinální masy identifikovalo dvoubuněčný brzlík o hmotnosti 90,8 gramu. Histologická analýza tkáňové biopsie mediastinální masy prokázala benigní hyperplazii thymu pravděpodobně sekundárně v důsledku neléčené hypertyreózy.
Pacient byl propuštěn domů ve stabilizovaném stavu s propranololem, propylthiouracilem a instrukcemi ke kontrole na endokrinologii.
Diskuse
Mediastinální biopsie pod obrazovou kontrolou je obecně bezpečný a minimálně invazivní postup. Existuje více přístupů a různé zobrazovací techniky – nejčastějšími metodami jsou ultrazvuk a počítačová tomografie (CT) pod kontrolou. Zobrazovací technika se volí na základě určitých charakteristik: klinických okolností, lokalizace útvaru, velikosti útvaru a základních podmínek bioptovaného vzorku. Před výběrem přístupu se zvažují anatomické a technické aspekty, cévní komponenty/životní orgány, výběr jehel a patologické aspekty.
Přímé mediastinální přístupy zahrnují paravertebrální, suprasternální, transpulmonální a extrapleurální . Perkutánní biopsie pod CT kontrolou má oproti jiným alternativním technikám několik výhod. Umožňuje přesnou lokalizaci cílové léze a přístup do mediastinálních oddílů, které nejsou snadno přístupné při mediastinoskopii nebo endobronchiální biopsii . Perkutánní biopsie pod US kontrolou má ve srovnání s biopsií pod CT kontrolou některé výhody, především možnost provádět ji v reálném čase s průběžným sledováním jehly během postupu a odběru vzorků. Pomocí US navigace lze také snadno dosáhnout více šikmých cest a její přenosnost předznamenává možnost provádět biopsie u lůžka kriticky nemocných pacientů .
Biopsie pod CT navigací poskytuje podrobné zobrazení a multiplanární reformulace, které pomáhají vyhnout se punkci cévních struktur a životně důležitých orgánů v hrudní dutině. Perkutánní transtorakální jehlová biopsie pod CT kontrolou je méně invazivní než mediastinoskopie a vyžaduje pouze lokální anestezii. Několik kontraindikací pro použití perkutánní transtorakální jehlové biopsie je podezření na hydatidovou cystu (absolutní kontraindikace), koagulopatie a těžce poškozená plicní funkce včetně bulózního emfyzému, plicní hypertenze nebo cévního tumoru .
U našeho pacienta byla identifikována přední mediastinální masa lokalizovaná v levé parasternální a retrosternální oblasti. U přední nebo střední mediastinální masy u pacienta bez kontraindikací se nejčastěji používá parasternální přístup s CT kontrolou. Při parasternálním přístupu se jehla zavádí přes parasternální svaly a mediastinální tuk do cílové léze. Mezi postupným posunem jehly se pořídí několik snímků ke kontrole trajektorie, aby se zajistilo, že vnitřní mamární cévy nejsou v cestě. Jehlou ráže 22 lze vstříknout fyziologický roztok nebo zředěnou kontrastní látku k rozšíření mediastina a vytvoření umělé extrapleurální dráhy pro umístění jehly . Po vytvoření bezpečného extrapleurálního okna se jehla 22 gauge odstraní a zavede se vodicí jehla s velkým otvorem (18 gauge nebo větší). Pomocí koaxiální techniky se přes vodicí jehlu provádí aspirace tenkou jehlou a core biopsie .
Mezi časté komplikace mediastinální biopsie patří vazovagální reakce, vzduchová embolie a rozsev nádoru . Závažné komplikace mediastinální biopsie pod CT kontrolou jsou neobvyklé a úmrtí jsou velmi vzácná . Mezi nejčastější život ohrožující komplikace mediastinální biopsie patří pneumotorax s výskytem v rozmezí 27-54 % po biopsii . Podle velké retrospektivní série je výskyt pneumotoraxu 20,5 % a výskyt pneumotoraxu vyžadujícího hrudní drenáž 3,1 % . Mezi další komplikace patří plicní krvácení s hemoptýzou nebo bez ní, hemotorax a hematom hrudní stěny . V případě hemotoraxu se v akutní fázi doporučuje hrudní drenáž a následně v subakutní fázi lytická terapie. Weinberg et al, přezkoumali celkem 830 hrudních biopsií z let 2006-2011 a zjistili, že celkem u 4 z 830 (0,5 %) došlo po biopsii k rozvoji hemotoraxu ve věku od 33 do 71 let. Žádný z pacientů neměl abnormální hodnoty koagulace nebo počtu trombocytů a za zmínku stojí, že u jednoho pacienta se příznaky objevily o více než 12 hodin později . Tomiyama a kol. v průzkumu japonských nemocnic zjistili, že pouze 0,092 % perkutánních biopsií plic vedlo k hemotoraxu . Yeowet, et al. zaznamenali pouze u 1 ze 680 (0,2 %) koaxiálních biopsií komplikaci v podobě hemotoraxu .
Krvácení bylo hlášeno z plicního zdroje nebo z poranění mezižeberní tepny. V žádném případě nebyl hlášen nález poranění perikardu s následkem srdeční tamponády.
V našem případě se u pacienta vyvinula srdeční tamponáda v důsledku hemoperikardu, což je vzácně hlášená komplikace mediastinálních biopsií . Předpokládáme, že jehla v našem případě vytvořila malou trhlinu v plicním řečišti a způsobila komunikaci mezi plicní tepnou a perikardem během extrakce tkáně. Naštěstí byla diagnóza stanovena rychle a pacient byl převezen k emergentní explorativní střední sternotomii.
Závěr
Perkutánní biopsie pod obrazovou kontrolou se rutinně používá k diagnostice mediastinálních lézí. Pro přesnou lokalizaci cílové léze se používá počítačová tomografie (CT) a ultrazvuková navigace. CT zobrazení je zavedeno jako nejlepší zobrazovací metoda pro navádění jehlové biopsie . Mezi faktory, které se podílejí na rozhodování o vhodném přístupu, patří klinické okolnosti, umístění, velikost cílové léze a komorbidní stavy . Nejlepší přístup pro perkutánní biopsii by měl být určen na základě přezkoumání předchozích snímků a anamnézy. Je nezbytné si uvědomit, že riziko komplikací se může lišit v závislosti na typu přístupu. Navzdory vysoké diagnostické přesnosti se vzácným výskytem komplikací je nezbytné určit nejbezpečnější přístup a být ostražitý vůči jakékoli komplikaci a v případě indikace poskytnout rychlou léčbu.
- Gupta S, Seaberg K, Wallace M (2005) Imaging-guided percutaneous biopsy of mediastinal lesions: different approaches and anatomic considerations. Radiographics 25: 763-786.
- Kulkarni S, Kulkarni A, Roy D, Thakur MH (2008) Perkutánní jádrová biopsie pod kontrolou počítačové tomografie pro diagnostiku mediastinálních mas. Annals of Thoracic Medicine 3: 13-17.
- Westcott JL (1988) Perkutánní transtorakální jehlová biopsie. Radiology 169: 593-601.
- Langen HJ, Klose KC, Keulers P, Adam G, Jochims M, Gunther RW (1995) Artificial widening of the mediastinum to gain access for extrapleural biopsy: clinical results. Radiology 196: 703-706.
- Hira L, Neyaz Z, Nath A, Borah S (2012) Perkutánní biopsie intrathorakálních lézí pod CT kontrolou. Korean J Radiol 13: 210-226.
- Bressler EL, Kirkham JA (1994) Mediastinální masy: Alternativní přístupy k jehlové biopsii pod CT kontrolou. Radiology 191: 391-396.
- Richardson CM, Pointon KS, Manhire AR, Macfarlane JT (2002) Perkutánní biopsie plic: přehled britské praxe založený na 5444 biopsiích. Br J Radiol 75: 731-735.
- Weinberg, B, Watumull, L, Landay M, Omar, H (2013) Variabilní prezentace hrudní biopsie související s hemothorakem. Universal Journal of Clinical Medicine 1: 22-27.
- Tomiyama N, Yasuhara Y, Nakajima Y, Adachi S, Arai Y, Kusumoto M, et al. (2006) CT-guided needle biopsy of lung lesions: a survey of severe complication based on 9783 biopsies in Japan. European Journal of Radiology 59: 60-64.
- Protopapas Z, Westcott JL (2000) Transtorakální hilová a mediastinální biopsie. Radiol Clin North Am 38: 281-289.