Salsola soda
Popel získaný spalováním sody S. lze rafinovat na produkt zvaný soda, který je jednou ze zásaditých surovin nezbytných pro výrobu sodnovápenatého skla, mýdla a mnoha dalších výrobků. Hlavní účinnou složkou je uhličitan sodný, pro který je dnes pojem „jedlá soda“ téměř synonymem. Zpracovaný popel sody obsahuje až 30 % uhličitanu sodného.
Vysoká koncentrace uhličitanu sodného v popelu sody se vyskytuje, pokud je rostlina pěstována ve vysoce zasolených půdách (tj. v půdách s vysokou koncentrací chloridu sodného), takže tkáně rostliny obsahují poměrně vysokou koncentraci sodných iontů. S. soda může být zavlažována mořskou vodou, která obsahuje přibližně 40 g/l rozpuštěného chloridu sodného a dalších solí. Při spalování těchto rostlin bohatých na sodík vzniklý oxid uhličitý pravděpodobně reaguje s tímto sodíkem za vzniku uhličitanu sodného.
Je překvapivé, že v rostlinných tkáních nacházíme vyšší koncentraci sodíku než draslíku; první prvek je obvykle toxický a druhý je pro metabolické procesy rostlin nezbytný. Většina rostlin, a zejména většina plodin, jsou tedy „glykofyty“ a při výsadbě v zasolených půdách trpí škodami. S. sodná a další rostliny, které byly pěstovány pro sodnou sůl, jsou „halofyty“, které snášejí mnohem slanější půdy než glykofyty a které mohou prosperovat s mnohem větší hustotou sodíku ve svých tkáních než glykofyty.
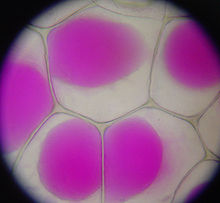
Biochemické procesy v buňkách halofytů jsou obvykle stejně citlivé na sodík jako procesy u glykofytů. Ionty sodíku z půdy nebo zavlažovací vody jsou pro rostliny toxické především proto, že narušují biochemické procesy v buňkách rostlin, které vyžadují draslík, což je chemicky podobný prvek alkalického kovu. Buňka halofytů, jako je S. soda, má molekulární transportní mechanismus, který zadržuje ionty sodíku v prostoru uvnitř rostlinné buňky zvaném „vakuola“. Vakuola rostlinné buňky může zabírat až 80 % objemu buňky; většina sodíku z rostlinné buňky halofytu může být zachycena ve vakuole, takže zbytek buňky má přijatelný poměr sodných a draselných iontů.
Kromě S. soda se soda vyrábí také z popela S. kali (další slanomilné rostliny), z rostlin skelnatky a z chaluhy, což je druh mořské řasy. Uhličitan sodný, který je rozpustný ve vodě, se z popela „vyluhuje“ (extrahuje vodou) a výsledný roztok se vaří nasucho, čímž se získá hotový produkt – uhličitan sodný. Velmi podobný postup se používá k získání potaše (hlavně uhličitanu draselného) z popela listnatých stromů. Protože halofyty musí mít ve svých tkáních také draselné ionty, obsahuje i nejlepší uhličitan sodný získaný z nich také trochu potaše (uhličitanu draselného), jak bylo známo již v 19. století.
Rostliny byly až do počátku 19. století velmi důležitým zdrojem uhličitanu sodného. V 18. století existoval ve Španělsku obrovský průmysl vyrábějící barillu (jeden z typů rostlinné uhličitanu sodného) ze slanomilných rostlin. Podobně ve Skotsku existoval v 18. století rozsáhlý průmysl výroby uhličitanu sodného z chaluh; tento průmysl byl tak výnosný, že vedl k přelidnění západních skotských ostrovů a podle jednoho odhadu se „kelpingem“ v letních měsících zabývalo 100 000 lidí. Komercionalizace Leblancova procesu syntézy uhličitanu sodného (ze soli, vápence a kyseliny sírové) ukončila éru zemědělství pro výrobu uhličitanu sodného v první polovině 19. století.


.