Syndrom akutní respirační tísně (ARDS)
Původní redakce – studenti projektu kardiorespirační terapie Glasgow Caledonian University.
Hlavní autoři – Geoff Boudreau, Matt Ross, Lucinda hampton, Kim Jackson a Adam Vallely Farrell
- Definice
- Etiologie
- Epidemiologie
- Patologický proces
- Klinický obraz a hodnocení
- Diagnostické postupy
- Lékařská anamnéza
- Fyzikální vyšetření
- Výsledky vyšetření
- Management / intervence
- Možné zásahy při ARDS
- Ventilátorová hyperinflace (VHI)
- Polohování do pronace
- Mechanická ventilace
- Inverzní poměrná ventilace (IRV)
- Ventilace s uvolňováním tlaku v dýchacích cestách (APRV)
- Vysokofrekvenční oscilace (HFO)
- Extrakorporální membránová oxygenace (ECMO)
- Inhalovaný oxid dusnatý
- Úloha fyzioterapeuta
- Závěry
- Zdroje
Definice
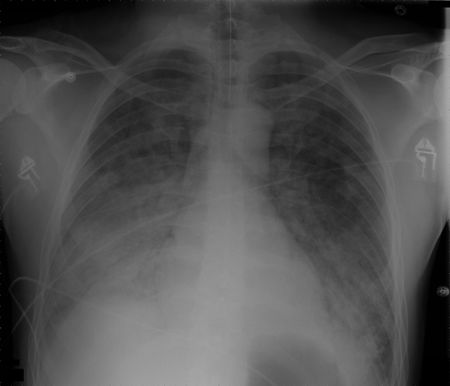
Syndrom akutní respirační tísně (ARDS)
- Je život ohrožující stav vážně nemocných pacientů, charakterizovaný špatnou oxygenaci, plicními infiltráty a ostrostí nástupu.
- Na mikroskopické úrovni je porucha spojena s poškozením kapilárního endotelu a difuzním poškozením alveolů.
- Nese s sebou vysokou mortalitu a existuje jen málo účinných terapeutických modalit pro boj s tímto stavem.
- Jakmile se ARDS rozvine, pacienti mají obvykle různý stupeň vazokonstrikce plicní tepny a následně se může vyvinout plicní hypertenze.
DefiniceARDS
- Akutní onemocnění, které začíná do 7 dnů od vyvolávající příhody a je charakterizováno oboustrannými plicními infiltráty a těžkou progredující hypoxemií při absenci jakýchkoli známek kardiogenního plicního edému.
- Definováno poměrem kyslíku v arteriální krvi pacienta (PaO2) k podílu kyslíku ve vdechovaném vzduchu (FiO2). Tito pacienti mají poměr PaO2/FiO2 menší než 300. Definice ARDS byla aktualizována v roce 2012 a nazývá se berlínská definice.

Etiologie
ARDS má mnoho rizikových faktorů.
- Plicní infekce např. výskyt ARDS při infekci COVID-19 se pohybuje mezi 17 % a 41 %
- Plicní aspirace
- Mezi mimoplicní zdroje patří sepse, trauma, masivní transfuze, utonutí, předávkování léky, tuková embolie, vdechnutí toxických výparů a pankreatitida (tato mimoplicní onemocnění a/nebo poranění spouštějí zánětlivou kaskádu vrcholící plicním poškozením).
Mezi rizikové faktory ARDS patří např:
- Pokročilý věk
- Ženské pohlaví
- Kouření
- Užívání alkoholu
- Operace aorty
- Kardiovaskulární onemocnění
- . operace
- Traumatické poranění mozku
Epidemiologie
- Odhady výskytu ARDS ve Spojených státech se pohybují od 64.2 až 78,9 případů/100 000 osoboroků.
- Dvacet pět procent případů ARDS je zpočátku klasifikováno jako mírné (1/3 přejde do těžkého nebo středního stupně) a 75 % jako středně těžké nebo těžké.
- Z přehledu literatury vyplynulo, že v letech 1994 až 2006 docházelo k poklesu úmrtnosti o 1,1 % ročně.
- Úmrtnost na ARDS závisí na závažnosti onemocnění, u lehkého, středně těžkého a těžkého onemocnění je 27 %, 32 % a 45 %.
- Prevalence osob trpících ARDS se v jednotlivých geografických oblastech značně liší. Ačkoli důvody těchto rozdílů nejsou jasné, někteří spekulují, že mohou pramenit z rozdílů v systémech zdravotní péče. Pro správnou evidenci a léčbu pacienta je nutná schopnost diagnostiky a rozlišení sekundárního stavu.
Patologický proces
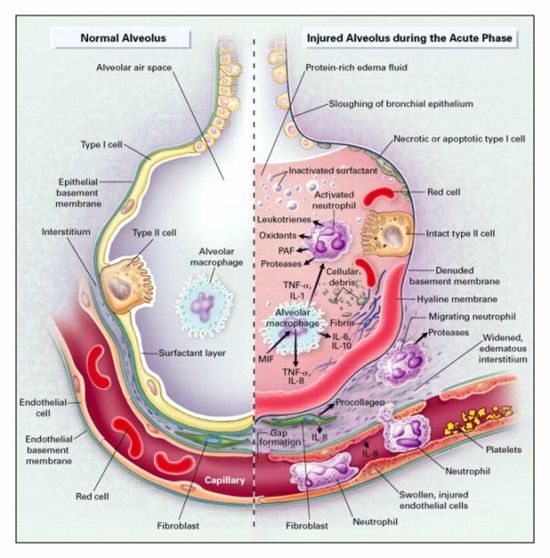
ARDS představuje stereotypní reakci na různé etiologie.
Probíhá v různých fázích
- První fáze – poškození alveolo-kapilární bariéry vedoucí k plicnímu edému. Poškození plicního epitelu a endotelu je charakterizováno zánětem, apoptózou, nekrózou a zvýšenou alveolokapilární propustností, což vede k rozvoji alveolárního edému a proteinózy. Dochází k obousměrnému úniku tekutin a proteinů do alveolu a také surfaktantových proteinů a alveolárních cytokinů do plazmy. Dochází k narušení epiteliální bariéry s proliferací alveolárních buněk typu 2, což vede k dysfunkci surfaktantu. alveolární edém zase snižuje výměnu plynů, což vede k hypoxemii.
- Proliferační fáze – vyznačuje se zlepšením funkce plic a hojením
- Závěrečná fibrotická fáze – signalizuje konec akutního procesu onemocnění. Obrat surfaktantu je výrazně zvýšený a tekutina, která vystýlá epitel, také zvýrazňuje fibrózní alveolitidu na počátku poškození plic
- Charakteristickým rysem obrazu poškození pozorovaného u ARDS je, že není jednotný. Segmenty plic mohou být postiženy závažněji, což má za následek sníženou regionální plicní poddajnost, která se klasicky týká více bazí než apexů.
- Tato intrapulmonální patologická diferenciace má za následek variantní odpověď na oxygenační strategie. Zvýšení pozitivního tlaku na konci výdechu (PEEP) sice může zlepšit difuzi kyslíku v postižených alveolech, ale může vést ke škodlivému volutraumatu a atelektraumatu sousedních nepostižených alveolů.
Toto 100sekundové video je dobrým úvodem do ARDS
Buněčné zapojení při ARDS:
- Neutrofily: Nejhojněji zastoupeny jak v epiteliální výstelce, tak v alveolárních histologických vzorcích. Ačkoli chemotaxický charakter neutrofilů procházejících epitelem nezpůsobuje poškození, jejich prozánětlivý charakter uvolňuje reaktivní formy kyslíku, cytokiny a řadu zánětlivých mediátorů, které přispívají k poškození bazální membrány.
- Alveolární makrofágy: Jsou nejčastějším typem buněk a spolu s intersticiálními makrofágy hrají důležitou roli v obraně. U pacientů s ARDS dochází k postupnému zvyšování počtu alveolárních makrofágů.
- Epitel: V alveolární epiteliální tkáni jsou obsaženy vysoce metabolicky aktivní alveolární buňky 2. typu. Poškozený epitel vede k dysfunkci surfaktantu
Klinický obraz a hodnocení
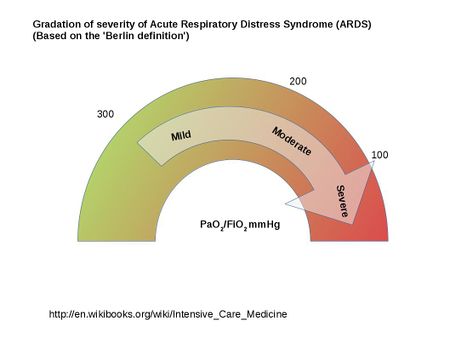
Syndrom je charakterizován :
- Rozvojem dušnosti a hypoxemie, která se postupně zhoršuje během hodin až dnů a často vyžaduje mechanickou ventilaci a péči na úrovni jednotky intenzivní péče.
- Anamnéza je zaměřena na zjištění základní příčiny, která onemocnění urychlila.
- Při rozhovoru s pacienty, kteří jsou schopni komunikovat, si často zpočátku stěžují na mírnou dušnost, ale během 12-24 hodin se dechová tíseň stupňuje, stává se závažnou a vyžaduje mechanickou ventilaci, aby se zabránilo hypoxii.
- Etiologie může být zřejmá v případě COVID 19, pneumonie nebo sepse. V jiných případech však může být pro identifikaci původce prvořadý i dotaz na pacienta nebo příbuzné ohledně nedávné expozice.
Fyzikální vyšetření může zjistit
- Akutní zánětlivou fázi: Trvá 3-10 dní a vede k hypoxémii a multiorgánovému selhání. Pacienti se obvykle projevují progresivní dušností, tachypnoí, cyanózou, hypoxickou zmateností a krepitací plic.
- Systémové příznaky (v závislosti na závažnosti onemocnění), např. centrální nebo periferní cyanóza v důsledku hypoxemie, tachykardie a změněný duševní stav.
- Navzdory 100% kyslíku mají pacienti nízkou saturaci kyslíkem. Auskultace hrudníku obvykle odhalí chrůpky, zejména bibasilární, ale často jsou auskulturovány v celém hrudníku.
- Hojení, proliferační fáze: Během této fáze je běžné zjizvení plic a pneumotoraka
Všimněte si, že v obou fázích se mohou vyskytnout sekundární systémové a hrudní infekce.
Diagnostické postupy
Podle National Heart, Lung and Blood Institute bude diagnóza stanovena na základě vyšetření anamnézy, fyzikálního vyšetření a výsledků testů.
Lékařská anamnéza
- Srdeční selhání v anamnéze
- Měl pacient nějaký přímý nebo nepřímý klinický rizikový faktor pro ARDS?
Fyzikální vyšetření
- Přidány dechové zvuky při auskultaci (např.g praskání)
- Auskultace srdce
- Cyanóza
Výsledky vyšetření
- Arteriální krevní plyny
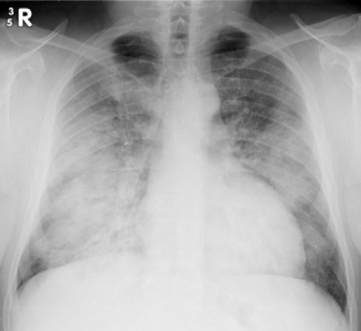
- Rtg hrudníkuray
- Krevní testy
- Kultivace sputa
- CT vyšetření
- Vyšetření srdečního selhání
Management / intervence
Naneštěstí, nebylo prokázáno, že by byl nějaký lék účinný v prevenci nebo léčbě ARDS.
Hlavní léčebnou strategií je podpůrná péče a zaměřuje se na
- Snížení frakce zkratu,
- Zvýšení dodávky kyslíku
- Snížení spotřeby kyslíku,
- Zamezení dalšího poškození.
Pacienti jsou mechanicky ventilováni, chráněni před přetížením tekutinami pomocí diuretik a je jim poskytována nutriční podpora, dokud není pozorováno zlepšení.
Způsob, jakým je pacient ventilován, má vliv na zotavení plic. Důkazy naznačují, že některé ventilační strategie mohou v souvislosti s ARDS zhoršovat alveolární poškození a udržovat poškození plic.
- Pozornost je třeba věnovat prevenci volutraumatu (vystavení velkým dechovým objemům), barotraumatu (vystavení vysokým tlakům na plato) a atelektraumatu (vystavení atelektáze).
Možné zásahy při ARDS
NB Zvažte poměr rizika a přínosu vašeho zásahu, zejména pokud jsou plíce tak křehké
- Odsávání (otevřené / uzavřené)
- Hyperinflace ventilátoru (VHI)
- Polohování (viz níže).
Ventilátorová hyperinflace (VHI)
Systematický přehled Andersona et al (2015) se domnívá, že manuální i ventilátorová hyperinflace mají podobný vliv na clearance sekretu, plicní compliance, zlepšují atelektázy a oxygenaci bez škodlivého rizika pro kardiovaskulární stabilitu. Po celou dobu zákroku by však měl být používán manometr a zvláštní pozornost by měla být věnována kontraindikacím.
Vzhledem k vysokým hodnotám PEEP, které jsou u pacienta s ARDS nutné k udržení náboru plic, je ideální používat k hyperinflaci ventilátor. VHI také umožňuje neustálé sledování a monitorování tlaků v dýchacích cestách, což umožňuje odpovídající titraci dodávky.
Polohování do pronace
Uložení pacienta s ARDS do pronace povede přibližně u 70 % pacientů k významnému zvýšení PaO2. Uložením pacienta do polohy na zádech dochází ke zlepšení náboru dorzální strany plic, což má za následek rovnoměrnější rozložení perfuze a zlepšení shody V/Q.

Důkazy ukazují, že polohování do pronace je prospěšné zejména u pacientů s těžkou hypoxémií/těžkým ARDS, přičemž dochází ke snížení úmrtnosti na JIP bez zvýšení komplikací v dýchacích cestách.
- Pacientovi s ujištěním vysvětlete, že bude v bezpečí, a získejte jeho souhlas, pokud je schopen komunikovat.
- Zavřete oči a chraňte je gelem nebo podložkou.
- Položte dlaně pacienta na stehna, palce vzhůru, lokty rovně a ramena neutrálně.
- Posuňte pacienta na okraj pomocí posuvného prostěradla.
- Převalte pacienta do boční polohy pomocí spodního prostěradla.
- Převalte pacienta do polohy na zádech.
- „Plavecká poloha“ – loket, ve kterém je hlava polootočená, by měl být ohnutý maximálně do 90°, aby nedošlo k natažení loketního nervu, a druhá paže vnitřně otočená do strany.
- Ujistěte se, že ženská prsa nebo mužské genitálie nejsou stlačeny.
- Pod každou holeň položte dva polštáře, abyste zabránili natažení peroneálního nervu, a umístěte je tak, aby nedocházelo k tlaku kolen a prstů od matrace.
Mechanická ventilace
V důsledku akutního nástupu hypoxemického respiračního selhání se zvýšenou dechovou prací je běžná mechanická ventilace. Patofyziologie ARDS a zejména jeho fibrózní aspekt znamená, že způsob a poskytování podpory vyžaduje pečlivé zvážení, aby nedošlo k ventilátorem indukovanému poškození plic (VLII)
U pacienta s ARDS je třeba snížit PEEP a dechový objem tak, aby odrážely dostupné části plic, které jsou k dispozici pro ventilaci. Pokud tomu tak není, může to vést k nadměrnému roztažení plic, tzv. volutraumatu v důsledku snížené poddajnosti plic. Opakované otevírání a zavírání alveolů během dechové inflace může také způsobit poškození plicní tkáně, známé jako alektotrauma. Pokud není mechanická podpora titrována na míru pacientovi, může alektotrauma i volutrauma zvýšit množství cytokinů v plicní tkáni, které se pak mohou dostat do systémové cirkulace a potenciálně vést k multiorgánovému selhání
Ačkoli je to možná příliš zjednodušené, níže uvedený graf se snaží zdůraznit optimální oblast pro ventilaci pacienta s ARDS. Předpokládá se, že dolní inflexní bod (LIP) je tlak, při kterém dochází k náboru plicní tkáně. Horní inflexní bod (UIP) je přibližný tlak, při kterém dochází k nadměrné distenzi alveolů, což může potenciálně vést k jejich poškození. Proto by nejoptimálnější poloha pro ventilaci měla být mezi oběma inflexními body, na nejstrmějším a nejkomplikovanějším aspektu křivky.

Moloney a Griffiths (2004)
Inverzní poměrná ventilace (IRV)
Tento způsob ventilace vyžaduje změnu normálního poměru nádechu a výdechu 1:2 na 1:1 nebo 2:1. V případě, že se jedná o ventilaci s opačným poměrem nádechu a výdechu, je nutné, aby se tento poměr změnil. Cílem tohoto způsobu ventilace je sice zvýšení aerace a kolaterální ventilace málo poddajných plic, ale zkrácení doby výdechu může vést ke zvýšení PCO2. Pokud však k hyperkapnické acidóze dochází pomalu, pak bude intracelulární acidóza dobře kompenzována, nicméně je třeba se vyhnout jakékoliv formě hyperkapnie u této s nebo u osob s rizikem vzniku zvýšeného intrakraniálního tlaku. Jedná se o tzv. permisivní hyperkapnii.
Nedávná, i když malá studie Kotaniho et al (2016) ukázala, že IRV zajišťuje přijatelnou výměnu plynů bez komplikací u 13 osob s ARDS.
Ventilace s uvolňováním tlaku v dýchacích cestách (APRV)
Tato forma mechanické ventilace zahrnuje podávání CPAP s přerušovanou uvolňovací fází. Předpokládá se, že dlouhodobé podávání CPAP udržuje dostatečný objem plic a alveolární nábor, kdy uvolňování má napomáhat odstraňování CO2. Vdechování začíná z příznivějšího poměru tlaku a objemu, čímž se napomáhá okysličování .
Vysokofrekvenční oscilace (HFO)
Při HFO je nastaven kontinuální distenční tlak (CDP) a pomocí oscilační pumpy jsou dodávány malé dechové objemy s vysokou frekvencí. Stejně jako ostatní dříve popsané se jedná o další formu protektivní plicní ventilace s konstantním náběrem plic. Systematický přehled Sud et al (2010) sice zjistil, že HFO může zlepšit přežití a pravděpodobně nezpůsobí poškození, ale bylo analyzováno pouze 8 studií s malým počtem pacientů a širokými intervaly spolehlivosti. Nebylo také zaznamenáno zaslepení hodnotitelů výsledků, což studie vystavuje riziku zkreslení.
Extrakorporální membránová oxygenace (ECMO)
ECMO lze použít u těch pacientů, kteří mají těžké respirační selhání, a používá se v případě, že konvenční léčba nemůže udržet adekvátní oxygenaci. ECMO může plně nahradit funkci plic, avšak vzhledem k různým komplikacím je třeba zvážit poměr rizika a přínosu.
ECMO se skládá z mimotělního krevního oběhu vytvořeného pomocí oxygenátoru a pumpy. Jsou vytvořeny dva cévní přístupy, jeden odvádí žilní krev a druhý infuzuje okysličenou krev. Po odběru krve z hlavní žíly se krev přečerpá přes okruh, který obsahuje oxygenátor, který krev okysličuje a odstraňuje oxid uhličitý. Krev se pak vrací zpět druhou kanylou.
Inhalovaný oxid dusnatý
Oxid dusnatý je nejen relaxantem hladkého svalstva odvozeného od endotelu, ale pomáhá také při neurotransmisi, obraně hostitele, agregaci krevních destiček a bronchodilataci. Inhalační oxid dusnatý může být podáván kontinuálně nebo pomocí přerušované inspirační injekce a za pozitivní odpověď se považuje zvýšení PaO2 o 20 %. U 40-70 % pacientů s ARDS dochází po inhalaci oxidu dusnatého ke zlepšení oxygenace a běžně se používá pouze u pacientů s těžkou hypoxemií jako dočasná záchrana.
Úloha fyzioterapeuta
Vstup fyzioterapeuta je často omezený a minimální často z důvodu potřeby vysokého PEEP a vysokých požadavků na kyslík. Vzhledem k tomu, že se jedná o intersticiální patologii, sekrece většinou nepředstavují problém. Léčba může spočívat pouze v polohování, např. vleže na zádech, aby se optimalizovala výměna plynů. Při praktických technikách je nutná opatrnost, protože je třeba zajistit, aby nedošlo ke ztrátě dlahového účinku PEEP ventilátoru. Pokud se sekrece stane problémem, zajistěte dostatečné zvlhčování spolu s dalšími technikami ke zlepšení odlučování sputa. Minimální odsávání přes ETT. Přehled současného stavu navrhuje vyhnout se opakovanému čištění dýchacích cest u kojenců a dětí s akutním plicním onemocněním.
Závěry
- Přestože je známo mnoho rizikových faktorů ARDS, neexistuje způsob, jak ARDS zabránit.
- U vysoce rizikových pacientů může pomoci pečlivé podávání tekutin.
- Měla by být přijata opatření k prevenci aspirace tím, že před krmením bude hlava lůžka ve zvýšené poloze.
- Strategie mechanické ventilace chránící plíce u pacientů bez ARDS, kteří jsou vysoce rizikoví, by pomohla zabránit ARDS.
Zdroje
- Cochrane Review: Cochrane Review: Recruitment manoeuvres for adults with acute respiratory distress syndrome receiving mechanical ventilation
- : Cochrane Review: Pressure-controlled versus volume-controlled ventilation for acute respiratory failure due to acute lung injury (ALI) or acute respiratory distress syndrome (ARDS)
- Cochrane Review: Cochrane Review: High versus low positive end-expiratory pressure (PEEP) for mechanically ventilated adult patients with acute lung injury and acute respiratory distress syndrome
- : Extrakorporální membránová oxygenace u kriticky nemocných dospělých
- Syndrom akutní respirační tísně. Berlínská definice
- ARDSNet: Souhrn protokolu mechanické ventilace